
自2015年WHO肺癌分类将免疫组化(IHC)引入临床病理分类模式以来, IHC在肺癌诊断中的重要性日益突出。除了区分小细胞癌和非小细胞癌(NSCC),患者选择的治疗方法与NSCC的组织学亚型直接相关,也与免疫组化结果有关,特别是对于低分化肿瘤。免疫组化的使用提高了肺癌分类的诊断准确性,但在某些情况下其鉴别仍然具有挑战性。识别肺癌的不同组织学分型和预后因素对不同患者选择最佳的个体化治疗方案,判断肺癌复发风险,具有极为重要的意义。结合Yasushi Yatabe等[1]在2019年发表的《肺癌免疫组化诊断的最佳实践建议》并结合临床实际,本期对免疫组化在肺癌诊断中应用的关键问题进行了阐述,有利于病理医生在诊断中正确使用免疫组化标志物。
肺癌免疫组化标志物检测要点
在过去十年中,免疫组织化学(IHC)领域取得了重大进展。染色技术的提高增加了敏感性和特异性。目前对肺癌患者的诊断,包括亚型的分型,以及靶向治疗等都与之相关联。因此,2015年WHO肺癌分类中首次将IHC引入分类模式,以反映肺癌的生物学特征,尤其是在小活检/细胞学标本和分化不良的肿瘤中,免疫组化的作用更加重要。以下10个问题是临床病理中经常碰到的问题,在此加以归纳和总结:
1.日常诊断中最常用的免疫标记组合是什么?
当非小细胞癌(NSCC)需要免疫组化分型时,TTF1和p40是金标准,如果没有神经内分泌分化(NE)的形态学特征,这两个标记在临床实践中通常是足够的。在鉴别鳞状细胞癌方面,P40优于p63。

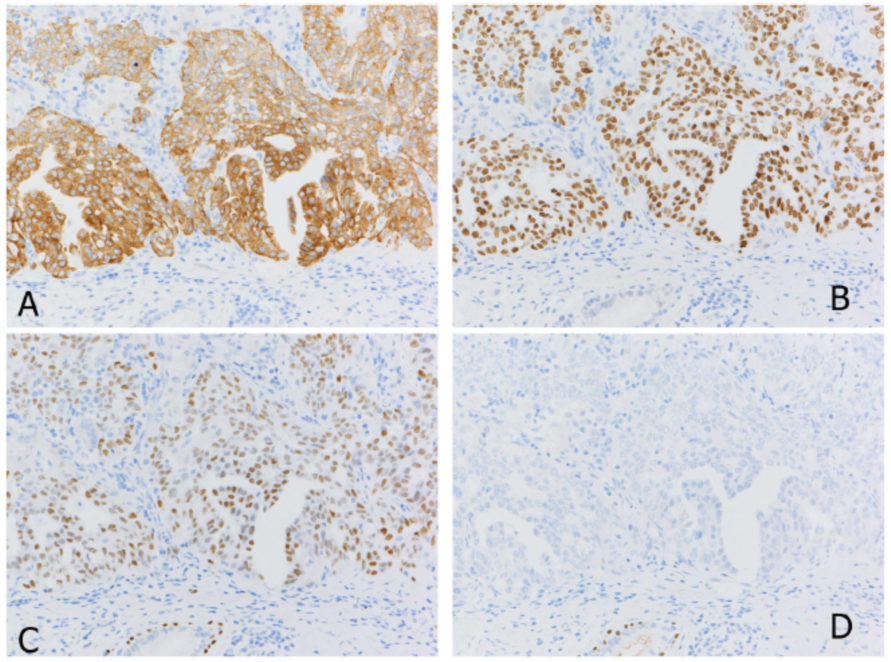
图1. ALK阳性的肺腺癌(A)。绝大多数ALK阳性肺癌的TTF1也呈阳性,如本例(B)。ALK阳性肿瘤的另一个特征包括p63(C)和p40(D)的不一致表达,当p63被单独用作鳞状细胞癌的标志物时,可能是一个陷阱。
2. TTF1和p40的阳性界值是多少?
TTF1的局灶阳性即可被认为是阳性,表明其为肺腺癌的可能性较高,而对于p40来说, 50%以上的肿瘤细胞核阳性才被认为是阳性。p40的局部/弱阳性不能诊断为鳞状细胞癌。另一个重要的问题是关于TTF1和p40/p63双阳性评价肺腺鳞癌的标准。首先,如果没有手术切除标本就不能做出这种诊断,在小活检中,如果有两种不同的细胞群存在,就会产生这种可能性。相反,同一细胞中的双阳性(TTF1和p40/p63)也不能定义腺鳞癌。研究显示,这种肿瘤可能应该被归类为NSCC,更倾向于腺癌。

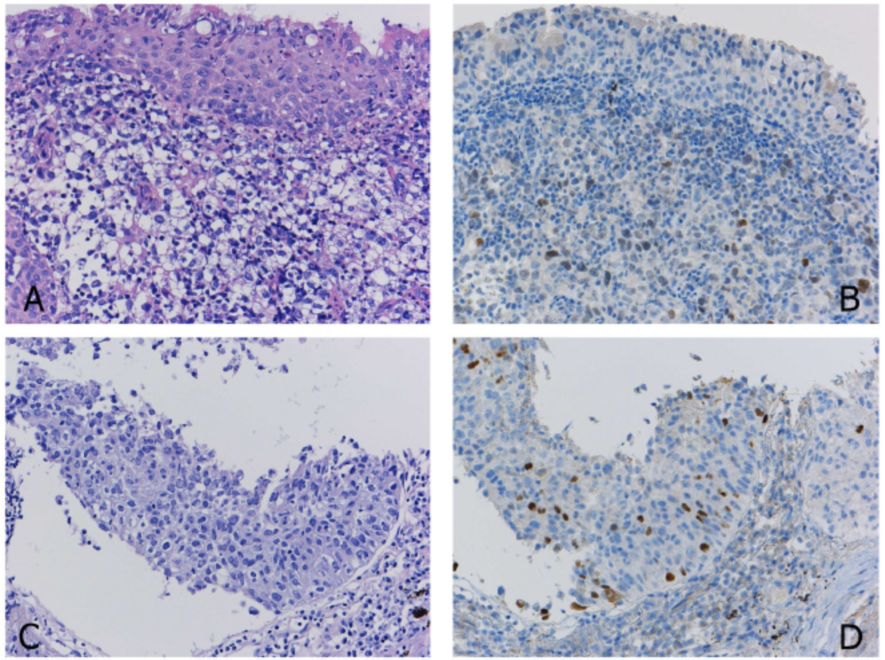
图2. 一个TTF1灶性阳性的病例。组织学上,肿瘤细胞没有显示出明确的形态学分化(A)。显示的TTF1染色(B)应被评价为阳性,因此该肿瘤被诊断为 "NSCC,倾向腺癌"。另一个病例也没有明确的形态学分化(C)。由于p40的阳性反应的定义是肿瘤细胞的50%或更多的阳性染色,所以p40的散在阳性(D)不能做出鳞状细胞癌的明确诊断(D)。
3. 在肺腺癌中,TTF1不同克隆之间是否存在染色差异(SPT24, SP141 and 8G7G3/1)?
TTF1的染色特异性因克隆号的不同而不同。在最常用的抗体中,8G7G3/1是诊断肺腺癌最特异的抗体。TTF1染色有两个重要作用:肺腺癌与鳞状细胞癌的鉴别诊断,以及原发性肺腺癌与非肺癌的鉴别,大多数情况下对这两者都具有特异性。然而,敏感性和特异性总是需要权衡的,在一些特殊类型的转移性肿瘤中,TTF-1仍可阳性表达。因此,即使在肺TTF1阳性腺癌中,对于病理医生来说,了解患者以前的肿瘤病史,特别是在形态特异的肿瘤中,寻找其他免疫组化标记物来确定其原发部位也是很重要的。

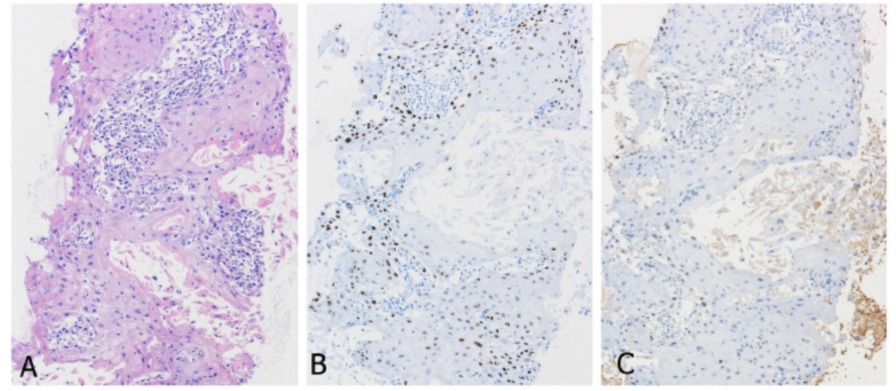
图3. 根据肺原发性鳞状细胞癌的抗体克隆,TTF1的表达(A,H&E染色)。克隆号SPT24染色阳性(B)与克隆号8G7G3/1的弱或阴性表达(C)形成对比。
4. CK7弥漫性阳性但TTF1和p40阴性的NSCC是否应被视为 "倾向是腺癌"?
CK7对腺癌的诊断没有特异性,这种标记在鳞状细胞癌中也可阳性。因此不鼓励在NSCC亚型中使用CK7。根据2015年WHO的分类,如果没有支持腺癌或鳞状细胞癌的形态学、粘蛋白染色或免疫组化标志物,在小的活检标本中,肿瘤应归类为NSCC,NOS。在没有TTF1或p40表达的情况下,CK5/6和CK7单独阳性时不能区分腺癌和鳞状细胞癌。

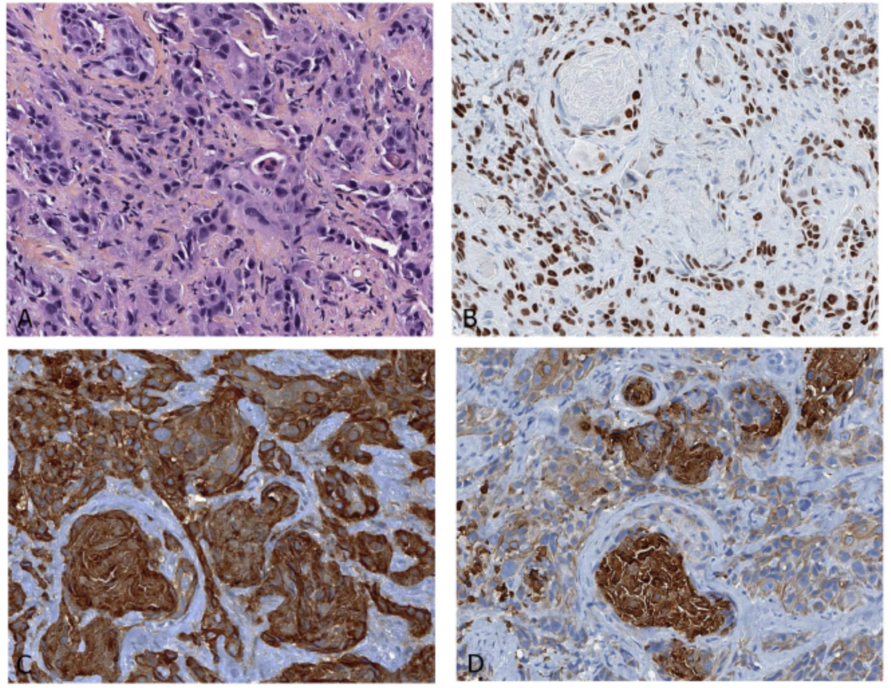
图4.支气管活检标本中鳞状细胞癌的细胞角蛋白表达(A)。p40(BC28 Ab)的核染色支持诊断(B)。细胞角蛋白7(OVTL12/30 Ab,C)和细胞角蛋白5/6(D5/16B4 Ab,D)均为阳性。
5. 什么时候应将神经内分泌(NE)标记应用于非鳞状细胞癌?
NE标志物应仅用于有NE形态学表现时才能应用。目前WHO的分类建议只有在出现NE形态学特征(器官样生长方式、缎带样结构等)时才应进行NE标记。大约10-30%的NSCC在光镜下没有明显的NE形态,但可能会遇到NE标志物阳性的情况。此类肿瘤可被称为“非小细胞癌伴NE分化”,但建议将手术切除的肿瘤主要分类为鳞状细胞癌、腺癌或大细胞癌(如适用),并对NE标志物的阳性比例做出说明。由于缺乏一致的数据支持在没有NE形态特征的情况下NE标志物阳性的临床意义,因此不建议对缺乏NE形态的肿瘤进行NE标志物染色。
6. 区分NE肿瘤与其他类型NSCC的最佳抗体组是什么?
嗜铬粒蛋白A(Syn)、突触素(CgA)和CD56是表达NE肿瘤的最佳组合。各抗体的染色意义因标本类型、组织学亚型及阳性反应的程度/强度而异。2015年WHO分类中给出了三种NE标记,包括嗜铬粒蛋白A、突触素和CD56。由于这些NE标记没有明确的阳性截断值,因此应结合形态学特征、样本类型(细胞学、活检或手术标本)和阳性反应程度进行判断。最近研究表明,hASH1在生物学上被认为是NE细胞分化谱系的一个标记,并能特异性地对NE肿瘤进行染色。多克隆神经元特异性烯醇化酶(NSE)具有高灵敏度,但由于特异性低而不再使用。最近对胰岛素瘤相关蛋白1(INSM1)的研究表明,这可能是对现有染色组合的一个理想补充,因为它对独立起源于器官和组织学的神经内分泌肿瘤具有高特异性和敏感性。虽然不清楚加入INSM1是否能改善目前推荐的CGA、SYN和CD56检测NE分化的总敏感性和特异性,但其核染色模式可能使判读更加直接。
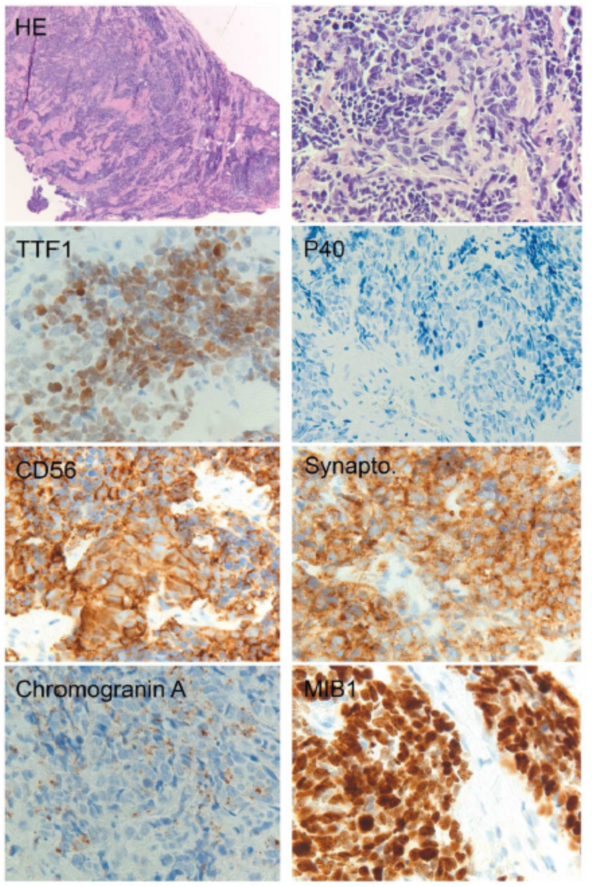
图5.肺类癌的典型免疫组化表达。注意肿瘤细胞的三个神经内分泌标志物均匀强染色和MIB1低表达。
7. 什么时候应该使用细胞增殖指数进行诊断?
Ki-67在肺癌中的主要作用是帮助区分类癌和高级别NE癌(大细胞神经内分泌癌和小细胞癌),特别是在小的或破碎的活检/细胞学样本中。Ki-67在区分典型和非典型类癌中的作用尚未确定,需要更多的研究。有几种Ki-67抗体可用于石蜡切片,但MIB-1克隆是抗原性修复后最广泛使用的抗体。目前不建议用Ki-67来进行鉴别诊断。Ki-67并没有被证明是一个不良的预后因素,尽管它在分化较差的肿瘤中往往会增加。根据组织学类型,预后的影响可能存在差异,其中增殖指数已被证明与腺癌的不良结果相关。然而,它可能与鳞状细胞癌的预后不相关。一种新的标记物——抗磷酸组蛋白H3(PHH3)作为有丝分裂特异性标记物已经在各种类型的肿瘤中进行了研究,但缺乏对肺癌的大规模研究。
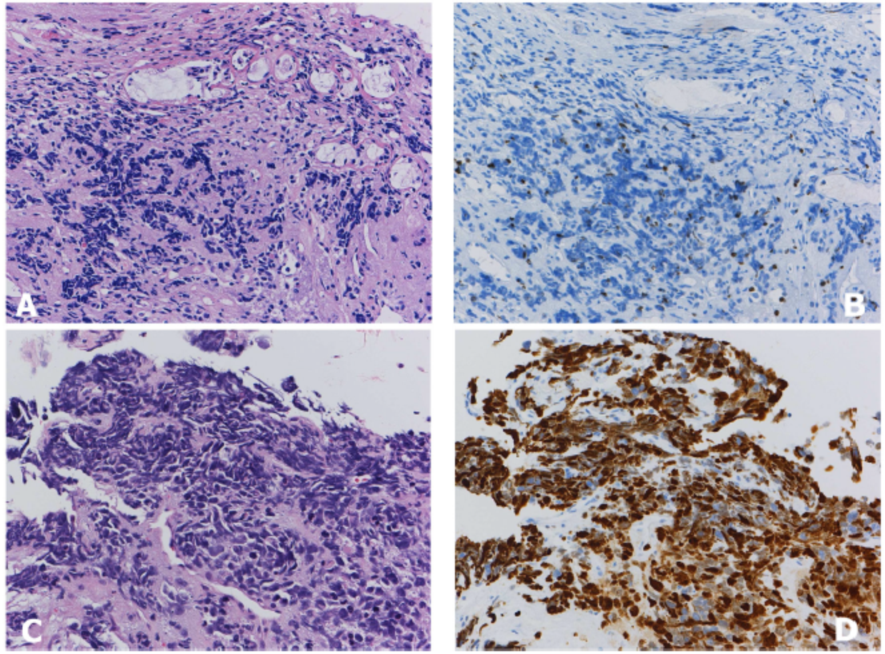
图6. 支气管活检常有挤压的肿瘤细胞,如图所示(A和C)。在这种情况下,如果是细胞学标本,Ki-67对诊断更有帮助,Ki-67染色(B和D)有助于类癌(A和B)和小细胞癌(C和D)的鉴别诊断。
8. IHC对罕见肺癌亚型(肉瘤、唾液腺来源肿瘤和NUT癌)的鉴别诊断是否有用?
目前,需要通过IHC以及分子检测来实现对罕见的肺癌进行明确诊断,并与形态相似的肿瘤进行区分。
肉瘤样癌
肺部的 "肉瘤样癌"是一个总称,包括梭形细胞癌、巨细胞癌和多形性癌(具有一个或多个常规癌成分的梭形/巨细胞癌),此外还有癌肉瘤和肺母细胞瘤。IHC的关键作用是将肉瘤样癌与肉瘤样间皮瘤、原发性或转移性肉瘤(如肾脏)区分开来,并排除其他类型肿瘤,如转移性黑色素瘤。角蛋白的表达在肉瘤样癌中可能是相当多变的。在大多数情况下,其表达是极其微弱和局灶性的,在小的活检标本中可能不明显。腺样和鳞状细胞分化的标志物TTF1和p40在肉瘤样癌中经常是阴性的,但在一部分病例中可能是阳性的。与肉瘤样癌相似,肉瘤样型间皮瘤对间皮标记物(WT1、Calretinin、D2-40)的表达通常为阴性或仅弱/局部阳性。尽管BAP1缺失通常有助于区分反应性间皮增生和恶性间皮瘤,但这种缺失发生在20%或更少的肉瘤样型间皮瘤中,同时也可能发生在其他恶性肿瘤中,如肉瘤样型RCC。癌变标志物的表达,包括Claudin-4、BER-EP4或B72.3,将支持肉瘤样癌的诊断,而不是间皮瘤,但与角蛋白相似,这些标志物的表达可能极其微弱和局灶。最近,GATA3在肉瘤样/蜕膜样型间皮瘤中100%表达,因此缺乏GATA3的表达可以用来排除肉瘤样型间皮瘤的诊断。值得注意的是,p16 FISH不能用于这种鉴别诊断,因为这两种肿瘤都可能缺失。在许多情况下,免疫组化表达可能对于诊断用处不大,最终的诊断需要结合临床-影像学信息和分子诊断结果。而角蛋白的局灶阳性不应作为支持肉瘤样癌的唯一诊断标准,反之,角蛋白表达阴性,特别是在小样本中,也不能倾向是肉瘤。
唾液腺型肿瘤
唾液腺型癌可以出现在肺部;在这种情况下,必须首先排除唾液腺原发肿瘤的转移。典型位置是支气管周围/支气管内。最常见的原发性肺部唾液型肿瘤包括粘液表皮样癌和腺样囊性癌。中间细胞和鳞状细胞中p40/p63表达,粘液染色的胞质内粘蛋白阳性,以及通过FISH显示MAML2重排即可以支持粘液表皮癌的诊断。SOX10在粘液表皮癌中通常是阴性的。肺部的主要鉴别诊断是腺癌;如果腺体成分中TTF1/Napsin-A的表达会支持腺癌诊断,而MAML2重排则支持粘液表皮样癌的诊断。对于腺样囊性癌,主要的鉴别诊断是与肺基底样鳞状细胞癌和其他唾液型肿瘤。腺样囊性癌表现为腔内上皮/肌上皮的双重组成,腔内细胞标记为低分子量角蛋白和c-Kit阳性,而肌上皮细胞标记为p63/p40、SMA和S100阳性。此外,大多数腺样囊性癌的IHC显示为MYB阳性,并含有MYB融合。罕见的唾液腺型癌在肺部也有报道。包括上皮-肌上皮癌(p63/SMA/S100阳性的外层肌上皮细胞)、腺泡细胞癌(SOX10、DOG1阳性)、透明细胞癌(最近在头颈部被重新命名为 "透明细胞癌"。p63/p40阳性,EWSR1融合),肌上皮癌(SOX10阳性,共同表达上皮标志物[角蛋白,EMA]+S100+多种肌源性标志物,p63,GFAP;EWSR1或FUS融合),以及与乳腺类似的分泌型癌(S100,乳球蛋白,GCDFP-15,SOX10,GATA-3,ETV6-NTRK3融合)。
NUT癌
睾丸核蛋白(NUT)癌是由15号染色体上存在的NUT基因重排所命名。一种高度特异性的NUT蛋白抗体已广泛商品化,它在NUT癌中显示出独特的斑点状核阳性。唯一能标记NUT的其他肿瘤是生殖细胞肿瘤,特别是精原细胞瘤;然而,它们的阳性通常是局灶性的,缺乏斑点状模式。值得注意的是,NUT癌可能有CD34阳性,这在与白血病浸润的鉴别诊断中很重要。其他鉴别诊断包括SWI/SNF染色质重塑因子缺陷的癌或肉瘤,它也显示出上皮样细胞的实体生长模式,往往部分具有横纹肌样特征。在一些报道中,这种肿瘤被报道为SMARCA4或SMARCB1缺失的癌或肉瘤。由于这类肿瘤是最近才被认识的,在目前的分类中还没有明确这类肿瘤的分类。
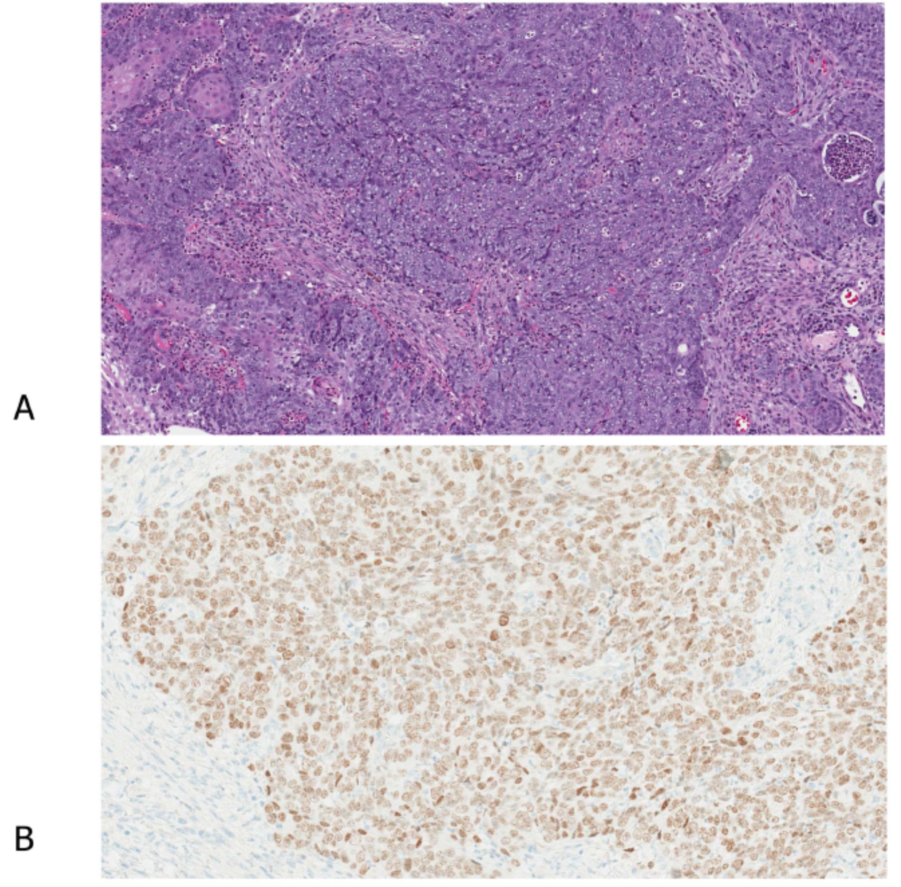
图7.NUT癌典型H&E表现:未分化的、原始的、具有局灶骤然角化的形态特征(A)。NUT蛋白免疫组化显示弥漫性核阳性,具有斑片状表达(B)。
9. 细胞学样本的中的哪种类型样本最适合进行免疫染色:细胞块、风干的涂片还是乙醇固定的涂片?去除染色的涂片可以被使用吗?
所有的细胞学样本,包括细胞块、乙醇固定的和风干的玻片,都可用于免疫染色。福尔马林固定的细胞块是最简单的,但在细胞学免疫染色中需要严格的方案优化、验证和质量控制。
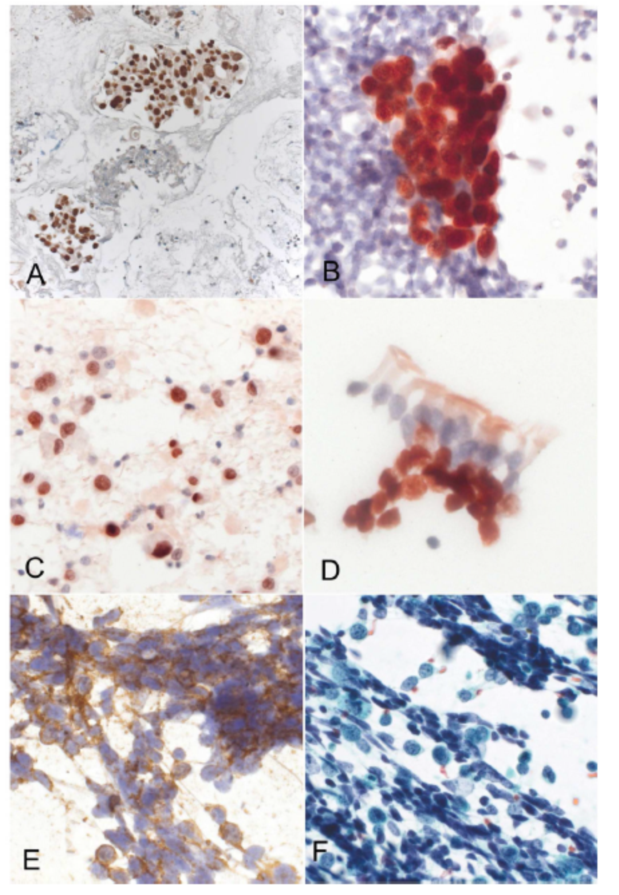
图8.细胞学标本的免疫组化染色。(A)细胞块标本中的TTF1阳性的腺癌(Ventana Benchmark XT免疫染色仪),对巴氏染色、乙醇固定、非细胞蜡块的免疫组化染色(Leica Bond自动免疫染色仪)。(B)TTF1阳性的腺癌(通过红色3-氨基-9乙基咔唑检测),(C)p40阳性的非角化鳞状细胞癌,(D)p40阳性的良性增生性的基底细胞(支气管刷细胞学),(E)CD56阳性小细胞癌与相应的巴氏染色标本(F)
10. 建议用哪些免疫组化套餐来区分肺的粘液腺癌和转移性癌:
目前还没有有用的标志物来区分肺黏液腺癌和转移性粘液腺癌。临床病史对于这类肿瘤的诊断至关重要。大多数肺浸润性粘液腺癌和其他具有粘液特征的肺腺癌,特别是缺乏TTF1表达的肺腺癌,HNF4α可以阳性。然而,HNF4α是原发肠道的分化转录因子,包括肝胆和消化道,都普遍表达这种转录因子。因此,HNF4α将无助于区分肺粘液腺癌和消化道及胰腺原发的粘液腺癌。在其他转移性粘液腺癌中,乳腺和卵巢原发的粘液腺癌可以通过其特定的标记物与肺部原发癌区分开来,包括乳腺的标记物GATA3和ER,卵巢的标记物PAX8。尽管文献中的结果令人满意,然而,实际情况下不能依赖这些标记物,因为不是所有的转移性肿瘤都是这些标记物的阳性。只有40%的卵巢粘液性肿瘤表达PAX8,表明这些抗体的鉴别诊断的敏感性很低。
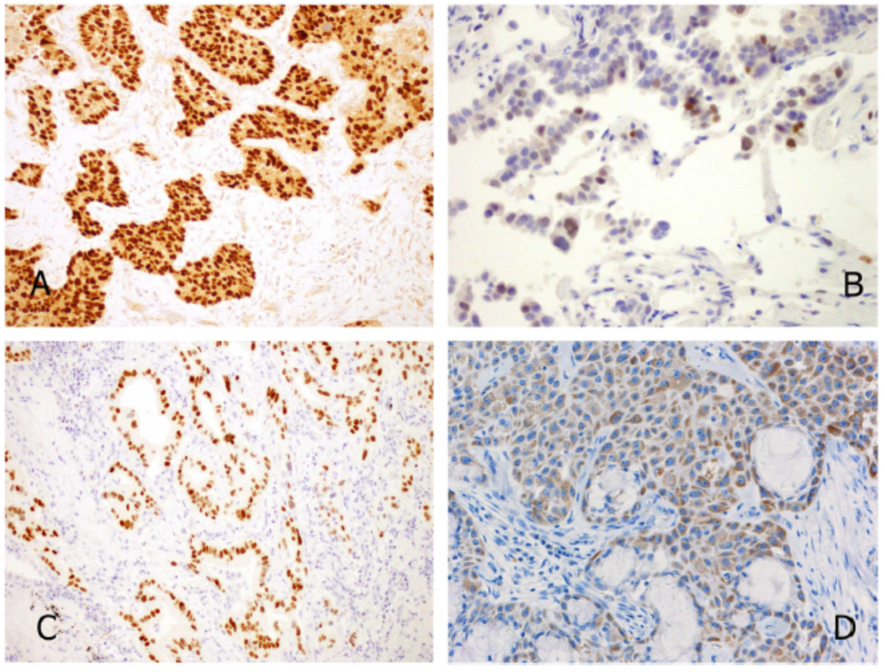
图9. 转移性肺癌的一些比较常见的鉴别诊断抗体和陷阱。子宫的转移性浆液性腺癌的PAX8(单克隆)阳性(A)。原发性肺腺癌中的局灶性ER阳性(B)。乳腺转移性腺癌的GATA3阳性(C)。肺部唾液腺型腺癌(粘液表皮细胞癌)的MGB1表达(D)。
我们选择了10个关于IHC的关键问题,与目前的临床病理实践最为相关。IHC现在是诊断病理学不可缺少的工具,但也有很多陷阱。因此,形态学应作为我们病理诊断的基础,上述所有建议只有在适当的临床背景下才有效。特别是,病理医生应该记住,临床病史,包括年龄、性别、吸烟状况,也提供了重要的诊断线索。在未来几年,新技术的发展和新抗体的出现可能会改变目前的诊断情况。与预测性生物标志物检测情况类似,诊断性IHC也与患者的治疗选择直接相关,因此临床及病理医生应确保所有患者在IHC的帮助下得到适当的诊断和治疗。
参考文献:
1. Yasushi Yatabe, Sanja Dacic, , Alain C. Borczuk, et al. Best Practices Recommendations for Diagnostic Immunohistochemistry in Lung Cancer, J Thorac Oncol. 2019, 14(3): 377–407




 苏公网安备 32011402010112号
苏公网安备 32011402010112号