鉴于已经存在的一些疾病实体在不同的唾液腺肿瘤之间显示出相当大的组织学和免疫组织化学特征的重叠,涎腺肿瘤WHO分类第5版仅接受有据可依的新的疾病实体。对于报道的肿瘤和变异的形态学,但缺乏共识支持和被独立的研究证实者均没有被包括在本版分类中。这样,本版分类中新的恶性疾病实体包括微分泌腺癌和硬化性多囊性腺癌,而良性肿瘤中增加了角化囊性瘤、闰管腺瘤和纹状管腺瘤。另外,硬化性多囊性腺瘤从非肿瘤性上皮性病变移到良性肿瘤分类中。
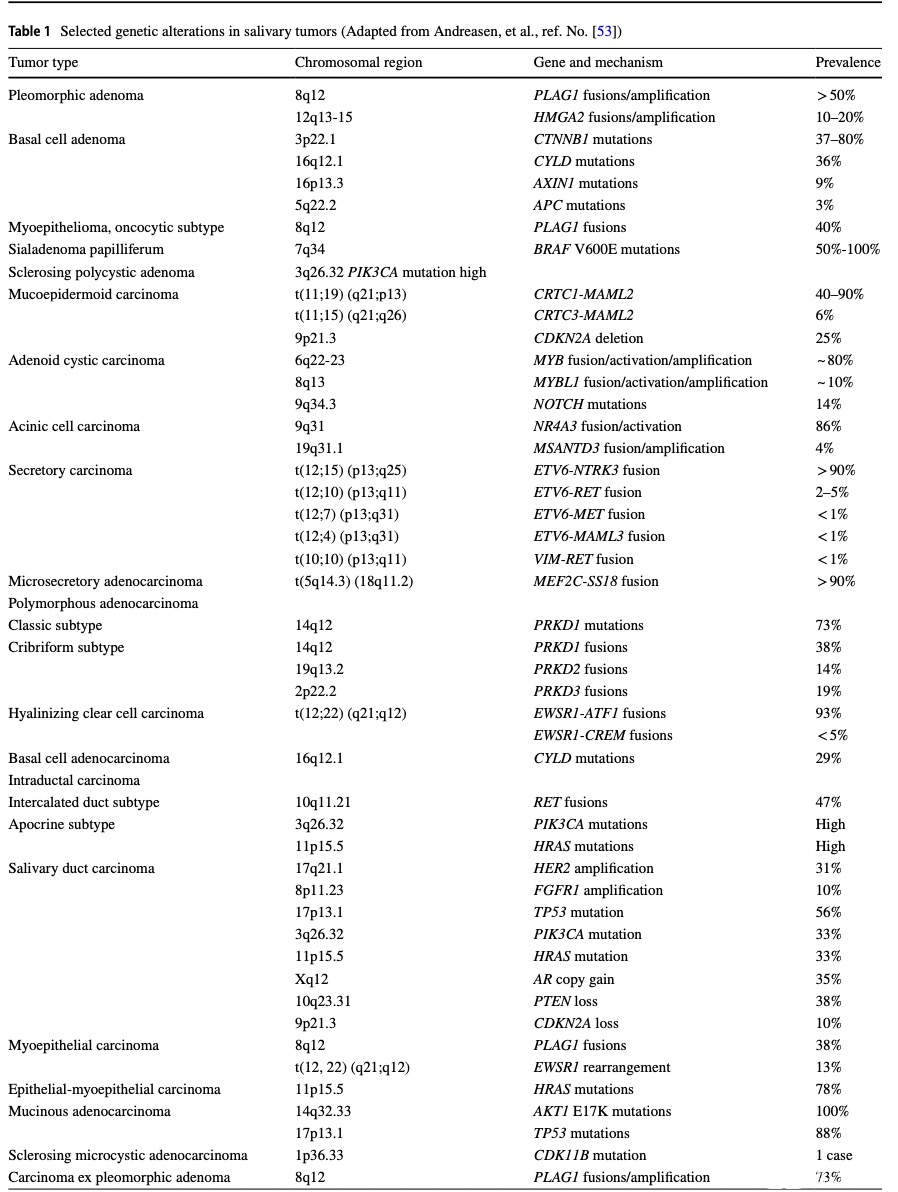
自上一版以来,分子数据被广泛报道,许多涎腺肿瘤显示具有肿瘤类型特异性重排(表1)。以下这些肿瘤的定义中包括了分子改变:黏液表皮样癌、腺样囊性癌、分泌性癌、多形性腺癌、透明变性透明细胞癌、黏液腺癌和微分泌腺癌。

大多数章节中包括了细胞学改变,推荐采用Milan系统。涎腺癌的组织学分级已经显示是一个独立的生物学行为预测因子,在最佳治疗中发挥重要作用,但大多数涎腺癌有其内在的生物学行为,试图采用广泛的分级系统并不推荐。已被证实的分级系统的癌的类型包括腺样囊性癌、黏液表皮样癌和腺癌,非特殊型。高级别转化(HGT)是涎腺癌内肿瘤进展的一个重要概念。表现为HGT的肿瘤显示侵袭性临床过程,明显不同于特定的肿瘤类型,因此,HGT现象被包括在合适的疾病实体描述中。
但在新版WHO蓝皮书中仍然有以下一些问题未被解决。
1)黏液腺癌(MA)分成乳头状、胶样、印戒和混合亚型,特征为各种结构中均有复发性AKT1 E17K的突变,提示产黏液的涎腺腺癌代表着一种组织学差异的单一疾病实体。导管内乳头状黏液性肿瘤(IPMN)是一种新兴的疾病实体,由具有低级别黏液性形态的导管中心肿瘤组成,它们具有MA常见的复发性AKT1突变。IPMN是否应该独立归类或作为一种潜在的前驱病变位于MA谱系内还不清楚。
2)导管内癌(IC)是一种涎腺恶性肿瘤,特征为完全或主要导管内的乳头状、筛状和实性增生。尽管名字为“导管内”,但明显浸润性生长伴肌上皮缺失能在IC中偶尔见到,然而,一项新近研究显示肌上皮细胞层是肿瘤的一部分,因此,ICs实际上可为双相性肿瘤而不是真正的原位肿瘤。
3)嗜酸细胞癌是否存在还没有共识。嗜酸细胞表现是许多不同涎腺肿瘤中遇到的一种常见改变。过去,完全由嗜酸细胞组成的癌常被诊断为嗜酸细胞癌。分子研究现在显示许多这样的肿瘤是其他涎腺癌的嗜酸细胞亚型,如果任何单纯性嗜酸细胞癌存在于不是其他癌的形态学亚型中是不确定的。因此,嗜酸细胞癌已被移到新兴的疾病实体章节中。
4)癌肉瘤在本版中仍然为一种独立的疾病实体,但不清楚肉瘤性成分代表着一种真性肉瘤还是上皮-间叶转化的结果。
第5版WHO中包括的新的疾病实体
硬化性多囊性腺瘤
硬化性多囊性腺瘤(SPA)是一种罕见的涎腺硬化性病变,具有特征性组织学表现组合,有些类似于乳腺的纤维囊性变、硬化性腺病和腺病瘤。SPA的组织学改变包括纤维化、囊性扩张、大汗腺化生、导管增生和具有丰富嗜酸性胞质颗粒的细胞组成的腺泡,以及不同比例的肌上皮细胞。最近研究不仅强烈支持SPA是一种肿瘤性病变,而且提示SPA、大汗腺IC和高级别浸润性SDC之间有密切关系。事实上,SPA可能代表着大汗腺IC,偶尔甚至浸润性SDC发展的一种前驱病变。
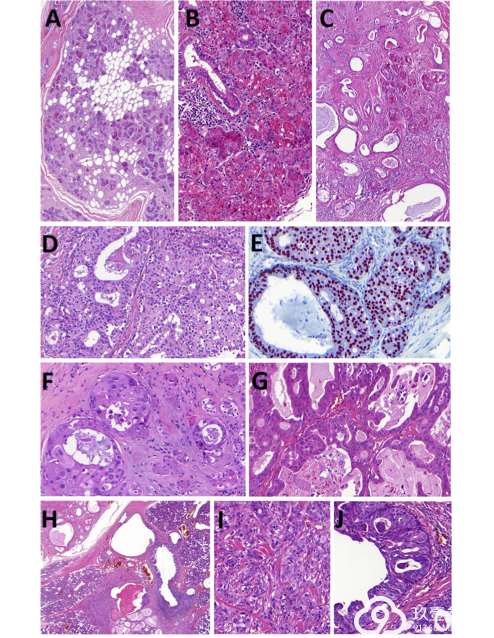
图1 硬化性多囊性腺瘤(SPA)。SPA是一种境界清楚和有包膜的肿瘤,由位于纤维性间质有时混杂灶性成熟脂肪组织中的导管和腺泡增生组成(图1A)。SPA的一个典型特征是存在具有丰富的、大的嗜酸性胞质颗粒的腺泡细胞(图1B)。导管结构被导管周围同心圆层状排列的透明变性间质围绕(图1C)。SPA常具有导管内上皮增生伴不同程度非典型。低级别非典型由表达SOX10的闰管样上皮组成(图1D, E)和高级别非典型性具有非典型和特征和复杂性生长方式,呈微乳头结构伴腔大汗腺上皮表达AR(图1 F,G)。起源于SPA的浸润性癌显示在图1H-J内。境界清楚主要为多囊性SPA通过纤维性假包膜与涎腺分开,见于图片的左上方(图1H),而在图1 I和J中分别显示浸润性导管癌和大汗腺导管内癌。
角化囊性瘤
角化囊性瘤是一种良性涎腺肿瘤,特征为多囊性腔隙,衬覆复层鳞状上皮,含有层状角化物和局灶性实性上皮巢。基本的诊断标准包括在多囊结构内衬覆无颗粒层的温和的复层鳞状上皮,存在界限明确的实性鳞状上皮细胞巢(图2)。所有报道的病例均位于腮腺内。鉴别诊断包括原发性和转移性鳞状细胞癌、黏液表皮样癌、化生性Warthin瘤和坏死性涎腺化生。
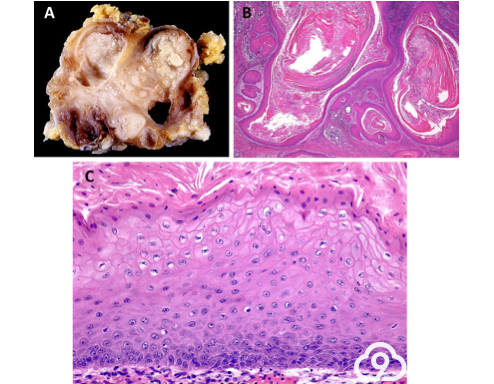
图2 角化囊性瘤。角化囊性瘤是由多囊性腔隙组成(图2A),衬覆复层鳞状上皮,含有层状角化(图2B)。鳞状上皮显示角化不全或表面正常角化,通常没有颗粒层(图2C)。(Toshitaka Nagao博士提供)。
闰管腺瘤
闰管腺瘤(IDA)是一种具有正常闰管细胞形态和免疫组化的双层导管的良性增生。IDAs与闰管增生一起是闰管增生性病变(IDL)的一部分,IDHs和IDAs均显示小的导管增生,胞质嗜酸性和小而温和细胞核。虽然肌上皮细胞采用肌上皮标志物能显示,但在常规HE染色切片上不明显。导管细胞显示弥漫性CK7阳性,局灶表达溶菌酶、ER,大多数病例弥漫性阳性表达S100。偶尔病变内可见腺泡细胞。IDA与IDH的区分被认为是基于存在一个不连续的、界限明确的、部分或完全有包膜的肿瘤,而不管背景涎腺实质内以前小叶结构。IDAs虽常因其他疾病切除而偶然发现,但少数病例可较大。IDLs与其他涎腺肿瘤如上皮-肌上皮癌、基底细胞腺瘤、基底细胞腺癌以及其他肿瘤的关系导致有些研究者认为IDL实际上可能是其他肿瘤的前驱病变。IDA的主要鉴别诊断是基底细胞腺瘤,后者趋向体积较大(典型>10mm),显示明显双层、明显梭形细胞间质和间质梭形细胞明显S100表达,而腔细胞表达弱和斑片状。
纹状管腺瘤
纹状管腺瘤是一种罕见的良性肿瘤,由具有细胞学特征类似于正常纹状管的单层细胞衬覆的导管组成(图3C, D)。不同于闰管腺瘤,纹状管腺瘤不含有肌上皮或基底细胞。肿瘤有包膜,由致密排列的导管组成,间质少或缺乏。肿瘤细胞嗜酸性,细胞膜明显类似于正常纹状管的条纹。免疫组化表达S100、CK7、CK7,不表达SMA。P63可显示单个阳性。偶尔肿瘤可显示核沟和核内假包涵体,类似于乳头状甲状腺癌的核特征。纹状管腺瘤的鉴别诊断包括嗜酸细胞瘤、闰管腺瘤、基底细胞腺瘤和小管腺瘤。缺乏双层结构、嗜碱性胞质和基底膜结缔组织可区分纹状管腺瘤和基底细胞腺瘤。小管腺瘤显示相互吻合的细胞索呈串珠状生长。嗜酸细胞瘤显示明显嗜酸性胞质,比纹状管腺瘤导管少,且有更多实性岛。最后,闰管腺瘤具有嗜碱性胞质和免疫组化上的肌上皮层。
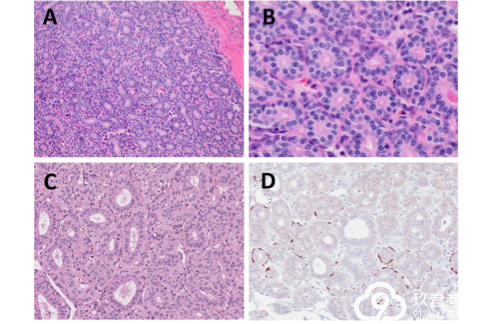
图3 闰管腺瘤(IDA)(图3A,B)和纹状管腺瘤(SDA)(图3C, D). IDA有具有正常闰管(图A)的细胞形态和免疫表型的双层导管组成。高倍镜显示梭形管腔周围肌上皮细胞层(图3B)。SDA由类似于正常纹状管(图3C)的单层细胞衬覆的导管组成,不含有肌上皮或基底细胞。仅偶尔腔周细胞表达SMA(图3D)。
微分泌腺癌
微分泌腺癌(MSA)是一种新认识的低级别涎腺腺癌,特征为具有独特的形态学和特异性MEF2C::SS18融合。该肿瘤的组织学特征为小的管腔和微囊,衬覆扁平闰管样细胞,含有丰富的嗜碱性腔内分泌物(图4)。细胞核大小一致,卵圆形,缺乏明显核仁。肿瘤细胞显示弥漫性S100、SOX10和p63,但不表达p40、calponin、SMA和mammaglobin。SS18基因重排是目前涎腺肿瘤该类型肿瘤独有,可采用FISH、PCR和NGS方法等检测。鉴别诊断包括腺样囊性癌、分泌性癌、多形性腺癌、分泌亚型肌上皮癌和腺癌,NOS。腺样囊性癌是一种双相性肿瘤,可通过免疫组化证实肌上皮标志物、CEA和EMA表达。分泌性癌缺乏黏液样间质,显示mammaglobin强阳性表达。多形性腺癌缺乏分泌性特征和黏液样间质,细胞显示更加丰富的胞质。肌上皮癌显示肌上皮标志物如calponin、SMA和p40表达,但不表达于MSA中。最后,所有这些肿瘤缺乏MEF2C::118基因融合。MSA预后较好,一项24例病例研究发现无1例发生复发、或局部或远处转移。
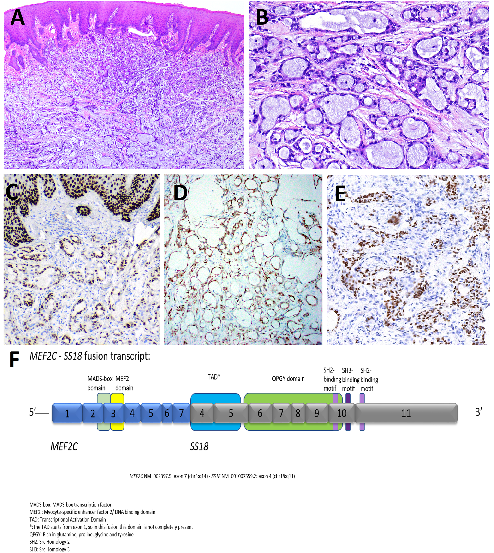
图4 微分泌腺癌(MSA)。MSA是小的小管和微囊组成,衬覆扁平闰管样细胞,含有丰富的嗜碱性腔内分泌物(图4A, B)。肿瘤细胞显示弥漫性p63(图4C)、S100蛋白(图4D)和SOX10(图4E)。MSA二代测序显示复发性MEF2C::SS18基因融合(图4F)。(Justin Bisho博士提供)。
硬化性微囊性腺癌
硬化性微囊性腺癌(SMA)是涎腺内一种罕见的恶性肿瘤,形态学特征类似于皮肤微囊性附件癌。SMA由小的浸润性条索和细胞巢包埋于厚的纤维或促纤维性间质内。肿瘤为双相性,腔内为温和的立方形导管细胞伴嗜酸性或透亮胞质和腔周扁平的肌上皮细胞。细胞核温和,圆形到卵圆形,偶见核沟。导管含有局灶性嗜酸性分泌物。常见神经周围侵犯,但核分裂象罕见(图5)。免疫组化腔细胞表达CK7,而腔周肌上皮细胞表达SMA、S100、p63和p40。鉴别诊断包括鳞状细胞癌(SCC)、玻璃变透明细胞癌、腺样囊性癌和肌上皮癌。缺乏角化、低级别细胞学和双相结构区分SMA与SCC。玻璃变透明细胞癌显示致密结缔组织间质和梁状结构,但缺乏管腔、分泌物和肌上皮细胞。肌上皮癌是一种单相性肿瘤无导管成分。腺样囊性癌具有双相性特征和易于发生神经周围侵犯,困难病例可进行MYB基因重排的分子检测可有帮助。
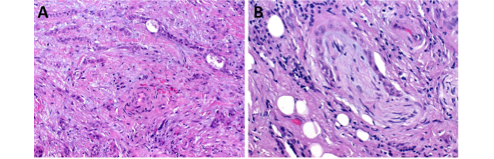
图5 硬化性微囊性腺癌(SMA)。SMA由小的浸润性条索和细胞巢组成,包膜于厚的纤维和促纤维性间质内(图5A)。常见神经周围侵犯(图5B)。(Abbas Agaimy博士提供)。




 苏公网安备 32011402010112号
苏公网安备 32011402010112号