引言
世界范围内,大部分发达国家癌症死亡率中肺癌占首位。尽管采用了多学科治疗晚期非小细胞肺癌(NSSCLC),但其总体生存率仍然很低。最近,已经开发出几种用于阻断免疫检查点的人源化单克隆抗体,并已证实对小细胞肺癌(SCLCs)治疗有效。程序性死亡分子1 (PD-1)和程序性死亡配体1 (PD-L1)之间的联系是这些单克隆抗体的靶点之一。抑制PD-1/PD-L1信号通路能提高机体抗肿瘤的免疫力,防止肿瘤细胞从宿主免疫应答中逃逸,为有效的肿瘤免疫治疗提供了广阔的前景。
经证实PD-L1阳性细胞数≥50%的病例用派姆单抗(抗PD1抗体)作为一线治疗与传统化疗相比,能显著提高进展期NSCLC的OS(总体生存期)及无进展生存期(PRS)。PD-L1 阳性细胞数≥1%的病例派姆单抗作为二线治疗也可获益。因此,患者的治疗选择中,PD-L1表达状态对派姆单抗治疗的效果至关重要。然而迄今为止,关于PD-L1的表达与各种临床病理因素之间联系的认识有限。因此,我们意图用切除的肺癌标本阐明PD-L1的表达和某些临床病理因素之间的联系。
材料和方法
本研究(登记号1461)经圣玛丽安娜大学医学院伦理委员会批准,并获得所有患者的知情同意书。选择2008年-2014年NSCLC患者的手术切除标本,由两名病理医生(M.T.和M.H.)分别对其HE染色切片进行单独复查,根据2015年7月版WHO分类确定其组织学类型和腺癌(Ad)的亚型。病理医生不参考临床资料来确定非小细胞肺癌的组织学类型及腺癌的亚型。选择的标本包括原位腺癌(AIS)11例,微浸润性腺癌(MIA)12例,贴壁为主型腺癌(LPA)10例,乳头为主型腺癌(PPA)13例,腺泡型腺癌(APA)14例,实体型腺癌(SPA)11例,浸润性黏液腺癌(IMA)4例,微乳头型腺癌(MPA)3例。除这78例腺癌外,本研究还选择了9例鳞状细胞癌(Sqs)和3例大细胞癌(Las)进行PD-L1表达的评估。所选样本包括37例男性和53例女性(年龄范围:46-81岁;平均年龄:66.5岁)。病例的TNM分期依据国际肺癌研究协会(IASLC)于2009.8公布的国际肺癌分期标准进行确定。临床分期中c-IA 64例、c-IB22例、c-IIA 2例、c-IIIA 2例。术后病理分期分别为p-IA53例、p-IB 13例、p-IIA 4例、p-IIIA10例、因下叶未行淋巴结清扫而分期未定的10例。术后平均随访期41±21个月(平均值±标准差(SD))。
免疫组织化学染色根据商家的说明书使用PD-L1试剂盒(PD-L1 IHC 22C3 dx;Dako,卡平特里亚,CA,USA)。此抗体是经美国食品药物管理局(FDA)批准的作为派姆单抗适用性治疗选择的伴随诊断试剂。简言之,从甲醛固定石蜡块上切取3μm的连续切片备用。切片经二甲苯及梯度酒精脱蜡至水。抗原修复使用Envition FLEX Target抗原修复液(Dako)97℃水浴20分钟。用过氧化氢阻断内源性过氧化物酶活性5分钟。冲洗缓冲液(Dako)冲洗切片后,用一抗覆盖组织。切片在室温下孵育30分钟。之后用缓冲液洗5分钟,3次, 然后加种属特异的一抗特异性抗鼠抗体孵育,再用含有二抗和辣根过氧化酶显色的即用型抗体孵育。最后切片用苏木素复染5分钟,封片。
PD-L1表达结果的判定
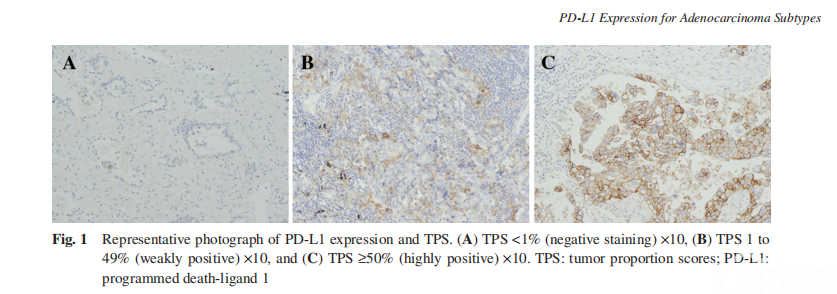
我们根据IASLC“肺癌PD-L1免疫组织化学检测”手册判读PD-L1染色结果。作者MH、TM和HN对PD-L1阳性细胞进行计数。阳性肿瘤细胞定义为完整或部分细胞膜染色。胞浆阳性的肿瘤细胞不计数。此外,肿瘤相关免疫细胞,如巨噬细胞阳性不计分。最后,评分以PD-L1阳性肿瘤细胞占肿瘤细胞总数的百分比来记录;肿瘤比例评分(tumor proportion score,TPS)。染色情况按TPS分为三组:<1%(阴性)、≥1%和<49%(弱阳性)、≥50% (强阳性)。所有TPS≥1%的肿瘤均为阳性表达。有代表性的染色图片如图1A-1c所示。
统计学分析
采用卡方检验对临床病理特征进行分层变量统计分析。采用Kaplan-Meier法分析OS和RFS(无复发存活期),采用log-rank检验(时序检验)单变量分析比较生存率的差异。采用Cox回归分析对生存期进行多变量分析。所有的统计分析使用EZR分析系统 (日本埼玉医科大学埼玉医学中心)进行分析,EZR是一款R语言图形用户界面(奥地利维也纳统计计算R语言会)的统计系统。更准确地说,EZR系统是一个常用于生物学统计的添加统计学功能的修改版本的R语言。p值<0.05提示检测结果具有统计学意义。
结果
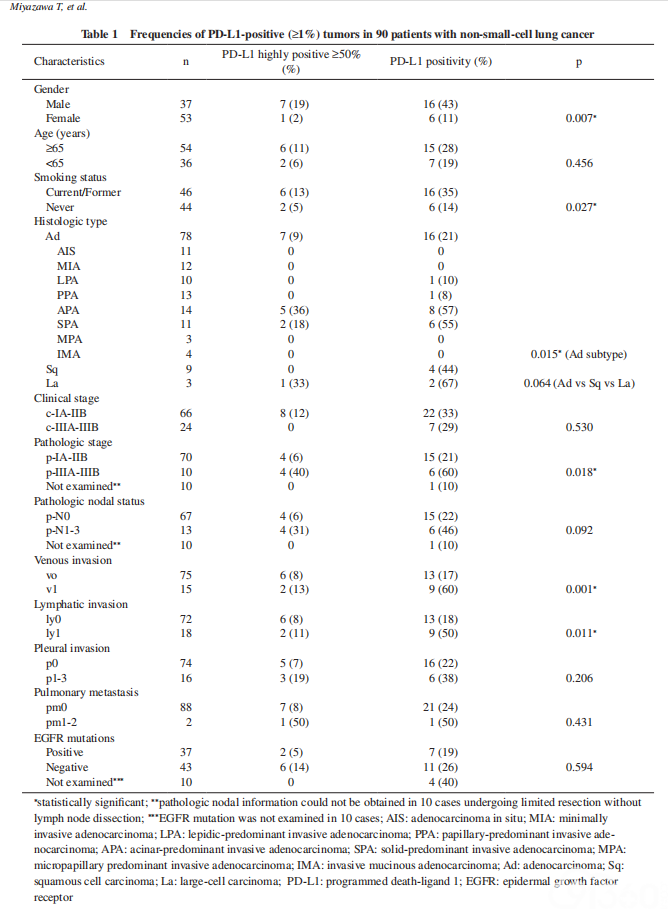
临床病理的特点和PD-L1阳性表达式(TPS≥1%)百分比的病例如表1所示。鳞癌(44%)和大细胞癌(67%)PD-L1 阳性比例高于腺癌(21%),统计学处于临界状态(p = 0.064)。腺癌的各亚型中,PD-L1阳性率分别为 APA(57%)、SPA(55%),高于AIS(0%)、MIA (0%),其他亚型分别为LPA(10%)、PPA(8%)、 MPA(0%)及IMA(0%),呈显著的不均匀分布(p = 0.015)。其他因素方面,PD-L1阳性率较高的因素包括男性(p = 0.001)、吸烟者(p = 0.027)、晚期IIIA(p = 0.018)、静脉浸润阳性率(p = 0.001)、淋巴管浸润阳性率(p = 0.011)。但是,年龄(≥65或 <65)、临床分期(c-IIIA-IIIB 或 c-IA-IIB)、病理中淋巴结的状态(pN1-3或pN0)、胸膜浸润(p1-3或 p0)以及EGFR突变与 PD-L1表达无相关性。
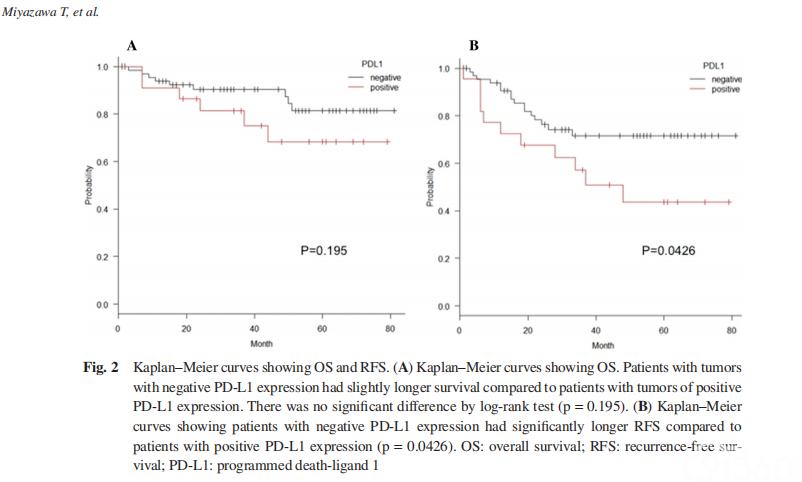
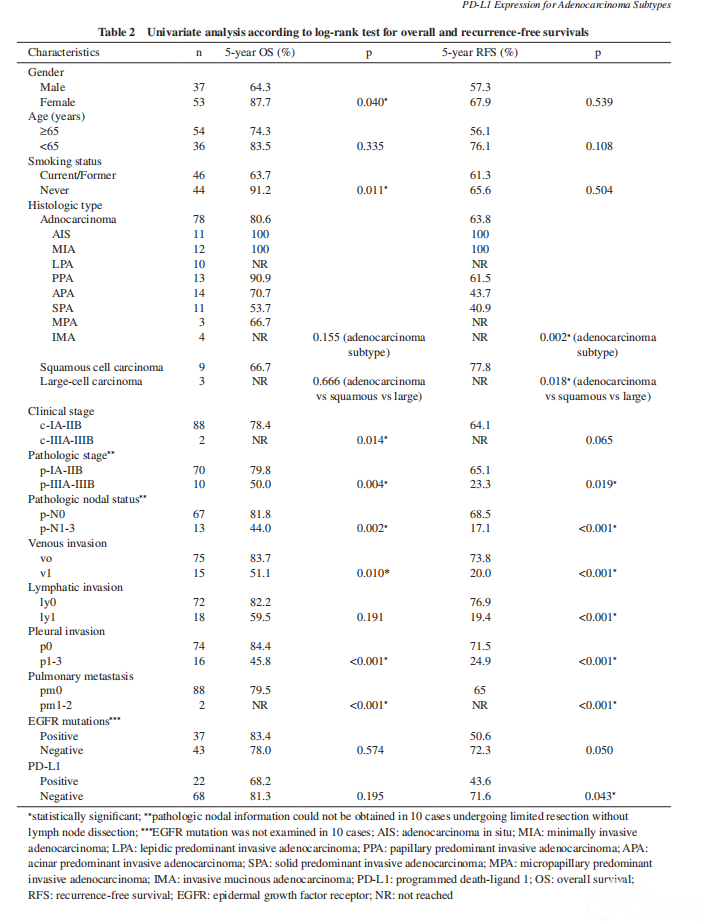
单变量分析表明,男性(p = 0.040)、吸烟习惯(p = 0.011)、进展期临床分期(p = 0.014)、进展期病理分期(p = 0.004)、病理的淋巴结转移(p = 0.002)、脉管侵犯(p = 0.010)、胸膜累犯(p < 0.001)、肺内的转移(p < 0.001)是OS差的预后因素(表2)。单变量分析腺癌的不同亚型(p = 0.002)之间、NSCLC不同组织学类型之间(p = 0.018)RFS显著不同。此外,RFS单变量分析表明病理进展期(p = 0.019)、病理有淋巴结转移(p = 0.001)、血管侵犯(p<0.001)、淋巴管侵犯(p<0.001)、胸膜累犯(p<0.001)、肺内转移(p<0.001)、PD-L1阳性(p = 0.043)是明显的不良预后因素。PD-L1阳性的OS 和RFS曲线见图2A和2B。
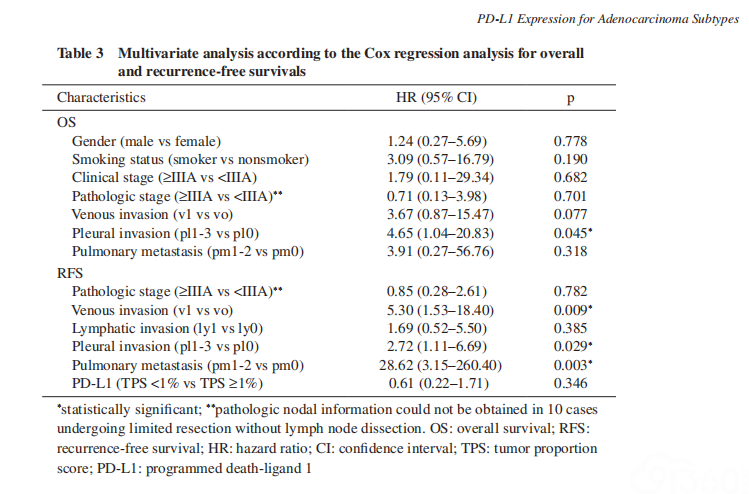
多变量分析提示胸膜累犯(p = 0.045)是OS的独立预后不良因素;血管累犯(p = 0.009)、胸膜累犯(p = 0.029)、肺内转移(p = 0.003)是RFS独立的预后不良因素(表 3)。
讨论
许多关于NSCLC中PD-L1蛋白表达的研究已被报道。但这些研究结果偶尔会相互矛盾,PD-L1表达的情况与各种临床病理因素的关系很难达成共识。之前的研究中观察的差异可能有几个原因。这些研究报告中的差异性可能是由于1)PD-L1抗体的使用;2)肿瘤细胞免疫组化染色的评价方法;3)阳性的定义;4)组织亚型所含的百分比,如Sq/Ad比例和Ad亚型所占的百分比;5)病变分期所占的百分比,如可切除/不可切除的比例、早期/进展期以及 6)在册患者的种族。为了降低免疫组织化学技术本身和评价方法的影响,本研究使用经FDA批准的派姆单抗的伴随诊断试剂,小鼠-22C3抗人PD-L1单克隆抗体,根据IASLC最近发布的指南,该抗体用于筛选适合派姆单抗治疗的患者。
已发表的几篇研究报道了PD-L1阳性肿瘤细胞的百分比和组织学类型之间的关系,但是每个研究中PD-L1阳性的评价标准不同。Janzic等评估了手术切除的肿瘤,报道称Sq(52%)中PD-L1阳性(TPS≥5%)病例比Ad(17%)中更多见。Scheel等观察了非小细胞肺癌的标本中鳞癌和腺癌(TPS≥1%)的阳性率均为34%,表明两个组织学类型之间的阳性率无差异。而Lin等用与Scheel等相同的标准比较PD-L1阳性率,结果表明鳞癌(46%)的阳性率高于腺癌(27%)。Cooper等也报道了PD-L1的表达情况(采用TPS≥50%),鳞癌的表达率为8%,大细胞癌为12%,腺癌的表达率为5%。我们的研究证实肺癌中鳞癌(44%)及大细胞癌(67%)PD-L1阳性 (TPS ≥1%)率比腺癌(21%)高,有统计学意义。
腺癌中,AIS(n = 11)和MIA(n = 12)均未发现PD-L1阳性的病例。目前认为AIS和MIA是生长非常缓慢的早期腺癌,这些亚型可能处于PD-1/PD-L1通路中未激活的状态。尽管LPA(n = 10)及PPA(n = 13)中只有2例阳性(9%)、APA(n = 14)及SPA(n = 11)中14 例(56%)阳性,提示这些亚型通常激活PD-1/PD-L1信号通路,抑制抗肿瘤免疫机制。PD-L1在腺癌中表达的研究很少。Zhang等分析了AIS(n = 1)、MIA(n = 6)、LPA(n = 8)、PPA (n = 27)、APA(n = 64)、SPA(n = 32)、 MPP(n = 1)、IMA(n = 3)及Enteric(n = 1)中PD-L1的表达情况,发现AIS及MIA中无表达(0%), LPA及PPA中表达率为46%,APA及SPA中的表达率为54%,从而得出结论AIS及MIA的PD-L1的阳性率低,而SPA的PD-L1表达率高。Igarashi等人使用原始的评分系统(H-score)对Ad各亚型中PD-L1的表达情况进行评估,其结果表明各亚型之间没有差异。本文的研究结果与Zhang等的研究结果一致。
PD-L1阳性与临床病理相关因素的关系还不确定。文献也做了PDL1在非小细胞肺癌中的表达和相关因素关系的多因素meta分析。但是meta分析的结果显示研究结果有相互矛盾的地方。Pan等结合9项研究中的1550例NSCLC病例,发现PD-L1高表达仅与肿瘤分化差有关,其它因素(性别、吸烟状况、组织学类型、浸润深度、淋巴结转移、肿瘤分期等相关因素)与PD-L1表达无关。相反,Zhang等结合47项研究中的11,444 例肺癌的研究结果显示PD-L1 在男性、吸烟者、鳞癌、高级别肿瘤、肿瘤体积较大、有淋巴结转移及进展期病变中的表达增高。我们的研究结果与Zhang等进行的meta分析结果类似,诸多的临床病理因素中提示有肿瘤进展因素的病例PD-L1表达增高。
关于PD-L1表达和EGFR突变的关系,研究结果之间也相互矛盾。部分研究显示EGFR突变的非小细胞肺癌中的PD-L1阳性率较高,部分报道则显示野生型EGFR非小细胞肺癌中的PD-L1表达较高。还有研究称PD-L1和EGFR之间没有关系。本研究也显示两者之间没有关系。
到目前为止,关于PD-L1表达在提示非小细胞肺癌预后的报道还有争议。先前的一些研究报道,PD-L1的高表达提示肺癌患者预后不良。Zhang等报道PD-L1表达是腺癌中总体存活率(OS)差的独立预测因子,该预测因子通过多因素Cox回归模型进行校正,包括年龄、性别、吸烟史、手术切除的类型、分化程度、TNM分期、组织学类型、突变的状态和围手术期化疗/放疗。与此类似,其它有关于非鳞状细胞癌和非小细胞肺癌研究结果也显示PD-L1阳性表达是总体生存率(OS)低的独立的预后不良指标。Lin等报道单个或多个组织学类型的早期切除的肺癌中PD-L1表达水平与生存率无关。Velcheti等报道了不同的结论,NSCLC中PD-L1的表达是独立于组织学亚型的预后良好的指标。另外5个meta分析研究中,有4个结果显示NSCLC患者中PD-L1表达与OS差有关。另一个meta分析报道NSCLC中PD-L1的表达无预后意义。Zhang指出PD-L1的表达和预后与人种有关;亚洲人PD-L1的表达与预后差有关,而非亚洲人群则没有相关性。本研究中,PD-L1阳性表达是单因素(而非多因素)分析中RFS的一个独立预测因子,且与OS无关,表明PD-L1表达的预后价值有限。
本研究有如下几个局限性。首先,入组病例数量相对较少,难以获得可靠结果。我们计划在下一个研究中加大样本量。第二,本研究不是前瞻性研究;因此,在某些组织学类型或Ad亚型病例中可能存在偏倚。由于我们使用的是存档的病理标本,石蜡包埋组织的保存时间可能会影响免疫组化染色的结果。然而在本研究中,我们发现2008年-2010年(10/40,25%)与2011年至2014年(12/50,24%)期间的组织PD-L1阳性表达没有统计学差异;p = 0.9127)。第三,术后随访观察的时间较短。
结论
本研究证实PD-L1蛋白的单克隆抗体22C3在NSCLC的不同组织学类型和Ad各亚型的表达均有差异。PD-L1阳性表达与性别、吸烟状况、病理分期、血管浸润、淋巴管浸润等临床病理因素有关。在唯一的单变量分析中,PD-L1阳性表达与RFS较短相关,提示PD-L1预后价值有限。我们需要用更大的样本量来进一步的研究从而证实我们目前的结果。
译者备注:这是一篇PubMed上搜索到的公开发表的全文,鉴于PDL1检测大热的今天,翻译了这篇文献。希望能够在各方观点中增加一点可参考的证据。鉴于篇幅限制,只翻译了文献的文字部分,图表及图片部分未做翻译。表1、表2比较庞大,为不影响整体阅读效果放在译文最后。不足之处请参考原文。




 苏公网安备 32011402010112号
苏公网安备 32011402010112号