大体检查:胰十二指肠切除标本,胰腺体积8*5*3cm,临床已剖开,切面见6.5*3.2cm肿物,灰白质韧,与周围组织界欠清。
形态学特征:肿瘤组织在胰腺内膨胀性生长,被纤维条索分隔成多结节状。肿瘤组织内血管丰富,局部可见坏死。肿瘤细胞排列呈腺泡状、梁索样、腺样及实性,胞浆较丰富嗜酸性细颗粒状,细胞核大小较一致,略呈空泡状,部分可见位于中位的小核仁,偶见核分裂像。
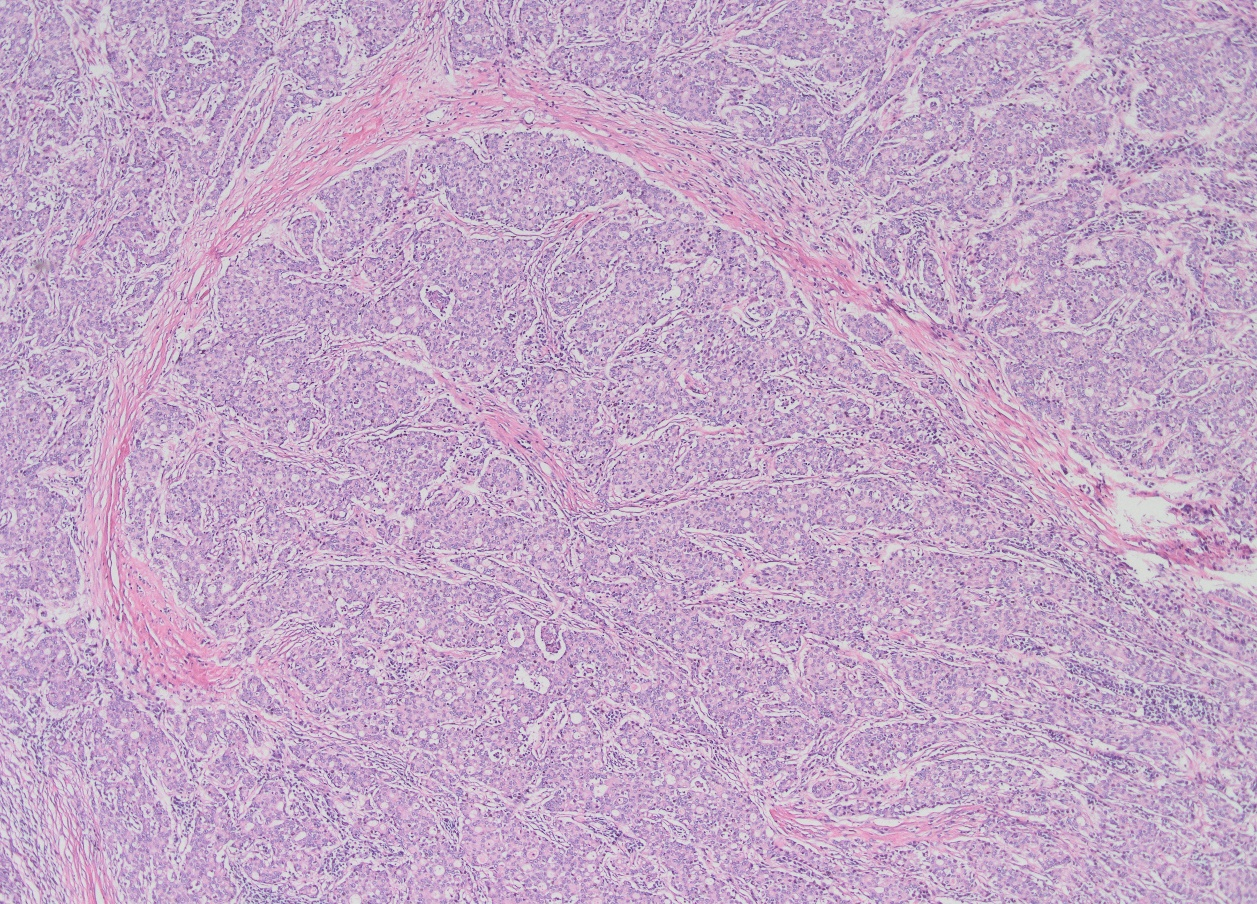
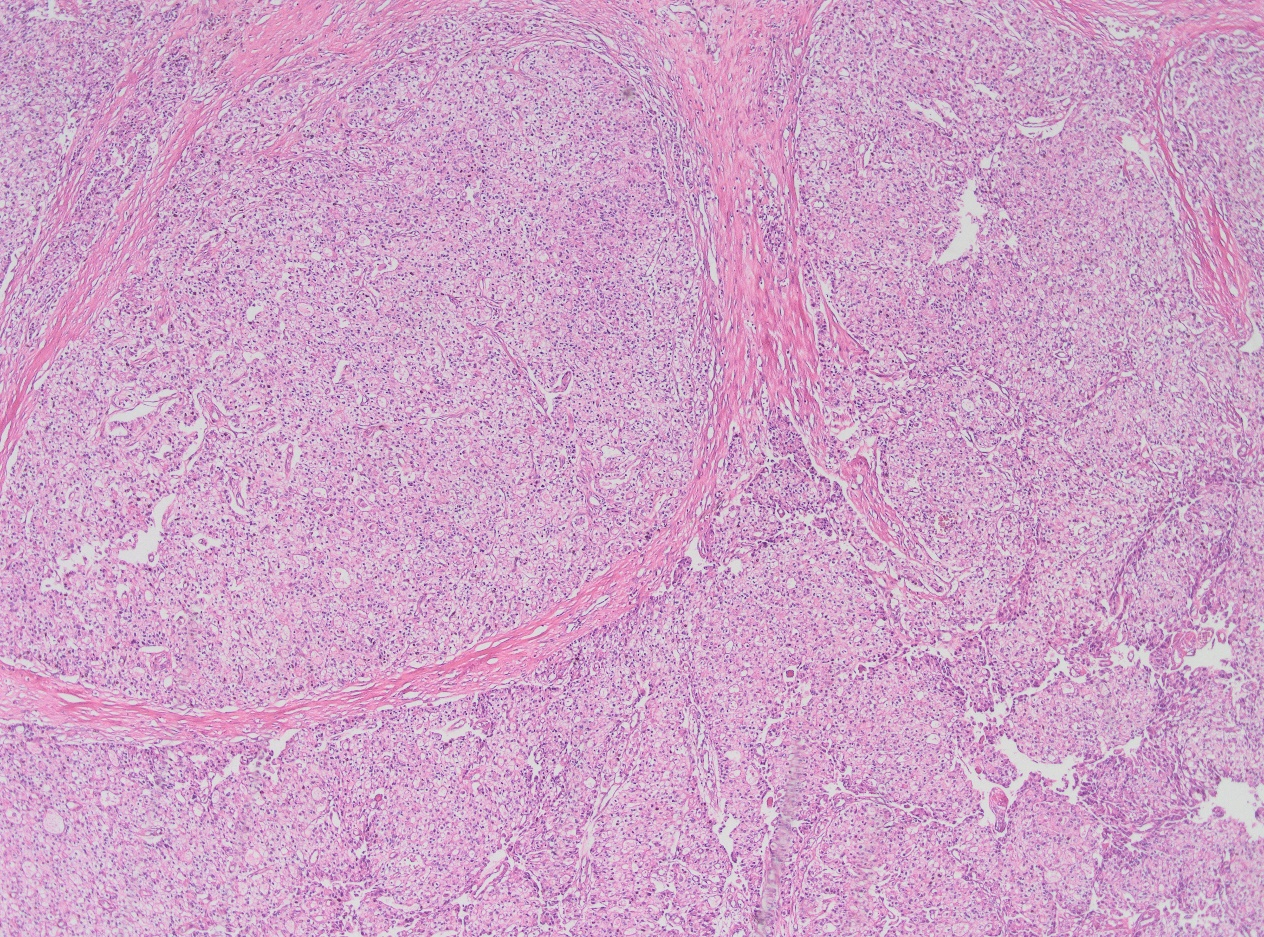
低倍镜下,肿瘤组织被纤维条索分割成大结节状,呈膨胀性生长,促纤维间质不明显。
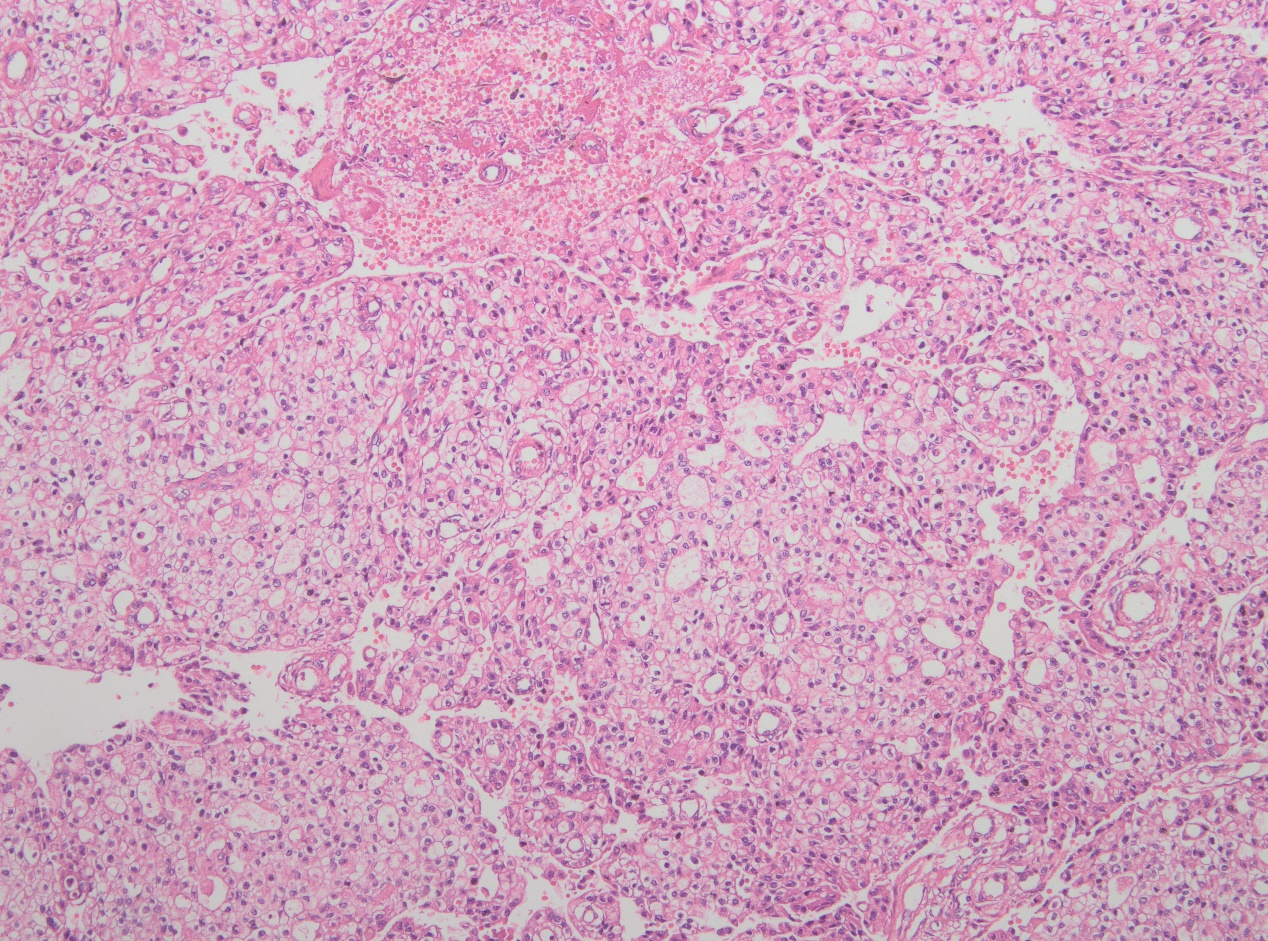
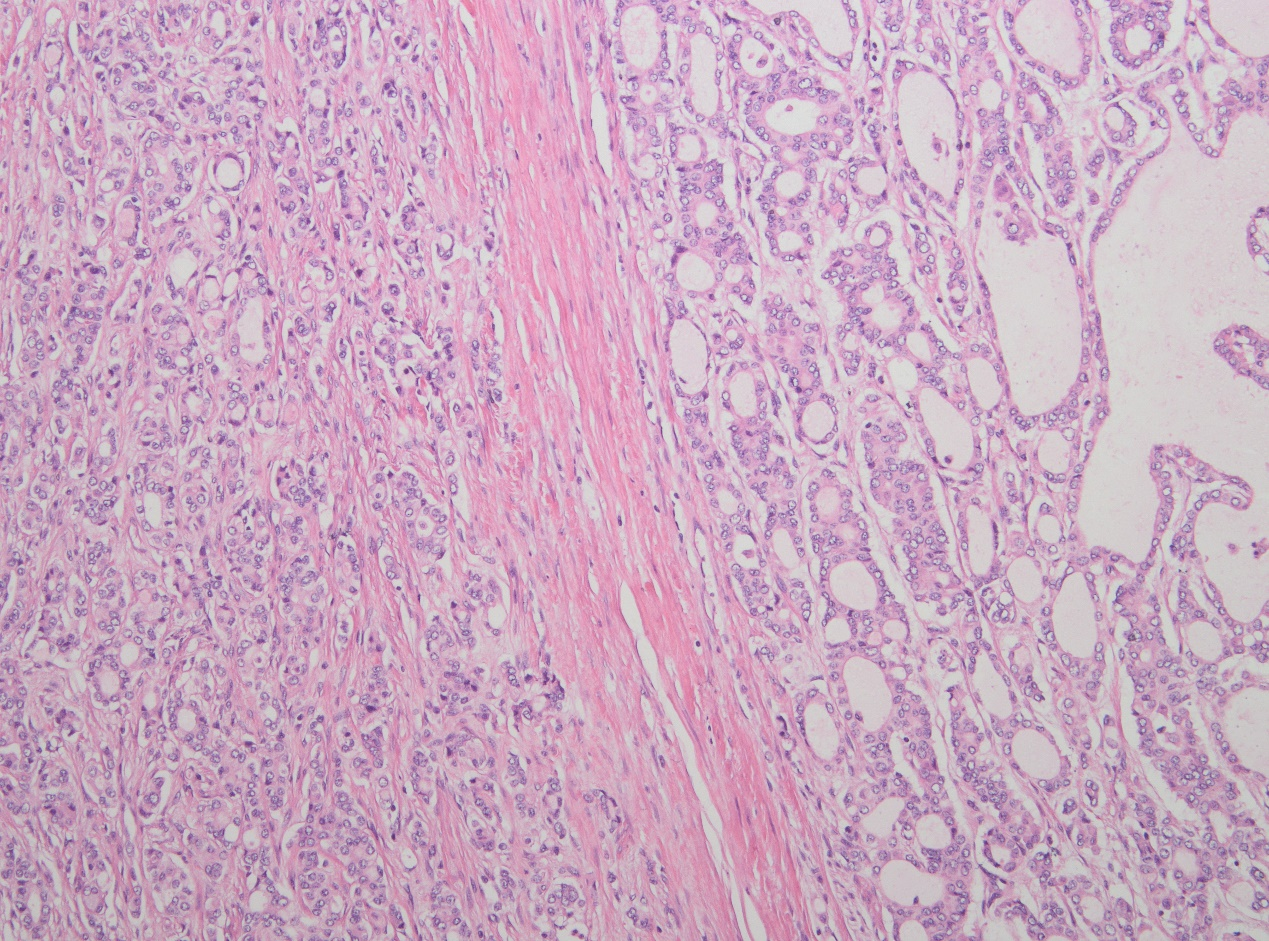
中倍镜下,肿瘤组织排列呈实性、梁索状、腺泡状及腺样,肿瘤组织内血管丰富,促纤维间质不明显。
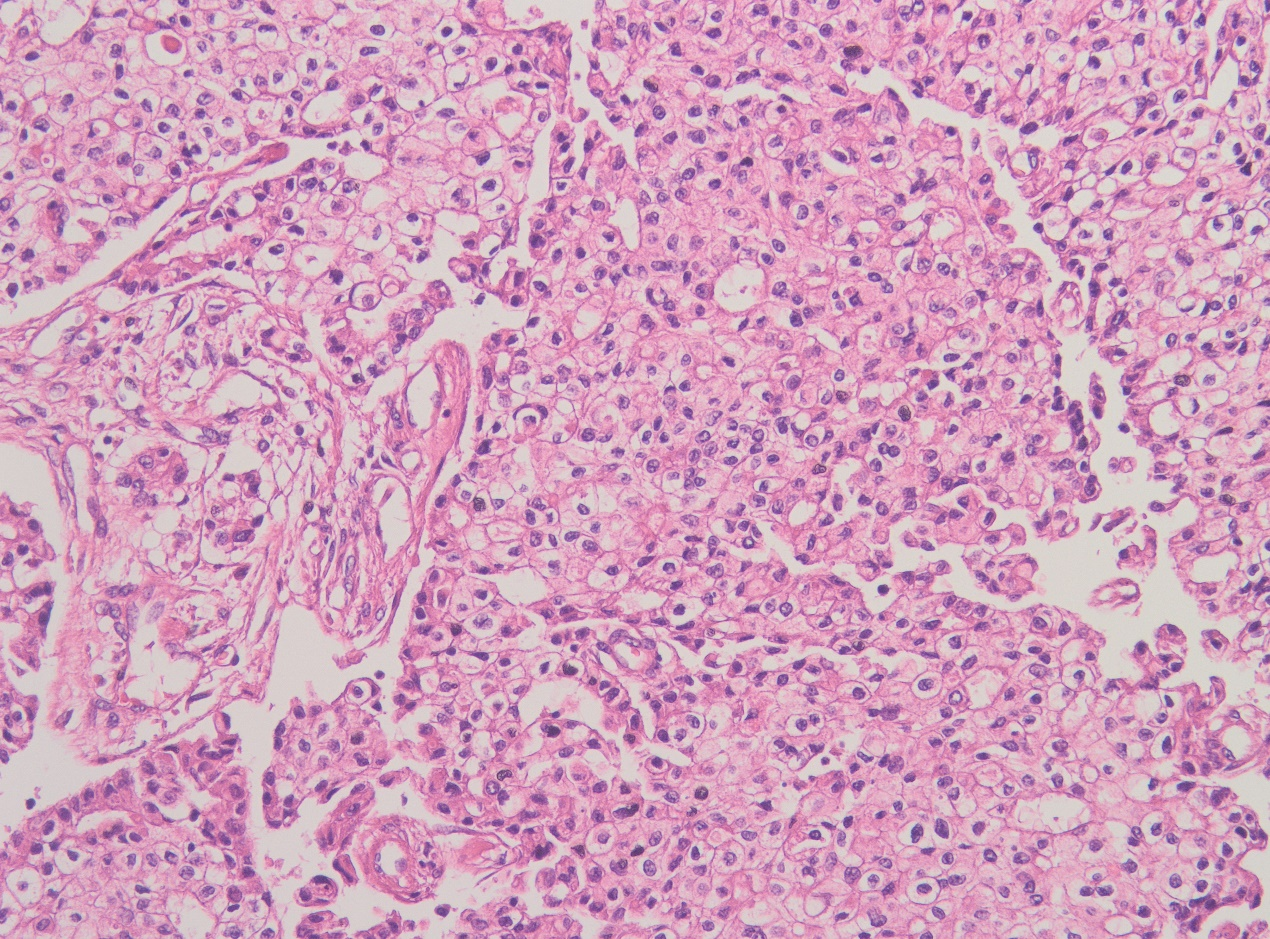
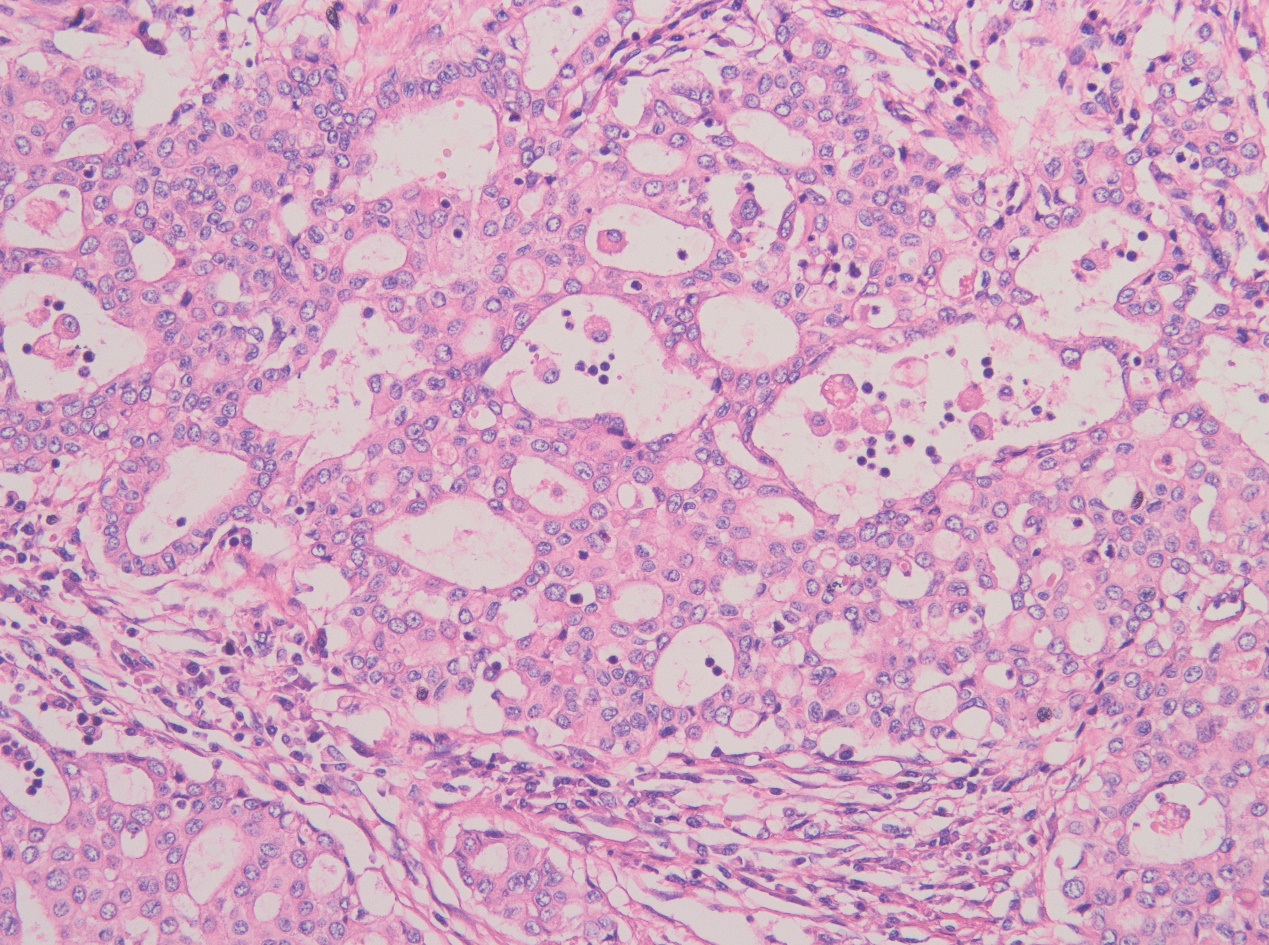
中高倍镜下,肿瘤组织排列呈实性、梁索状、腺泡状及腺样,肿瘤细胞胞浆较丰富,嗜酸性细颗粒状,细胞核异型性不明显,大小较一致,略呈空泡状。
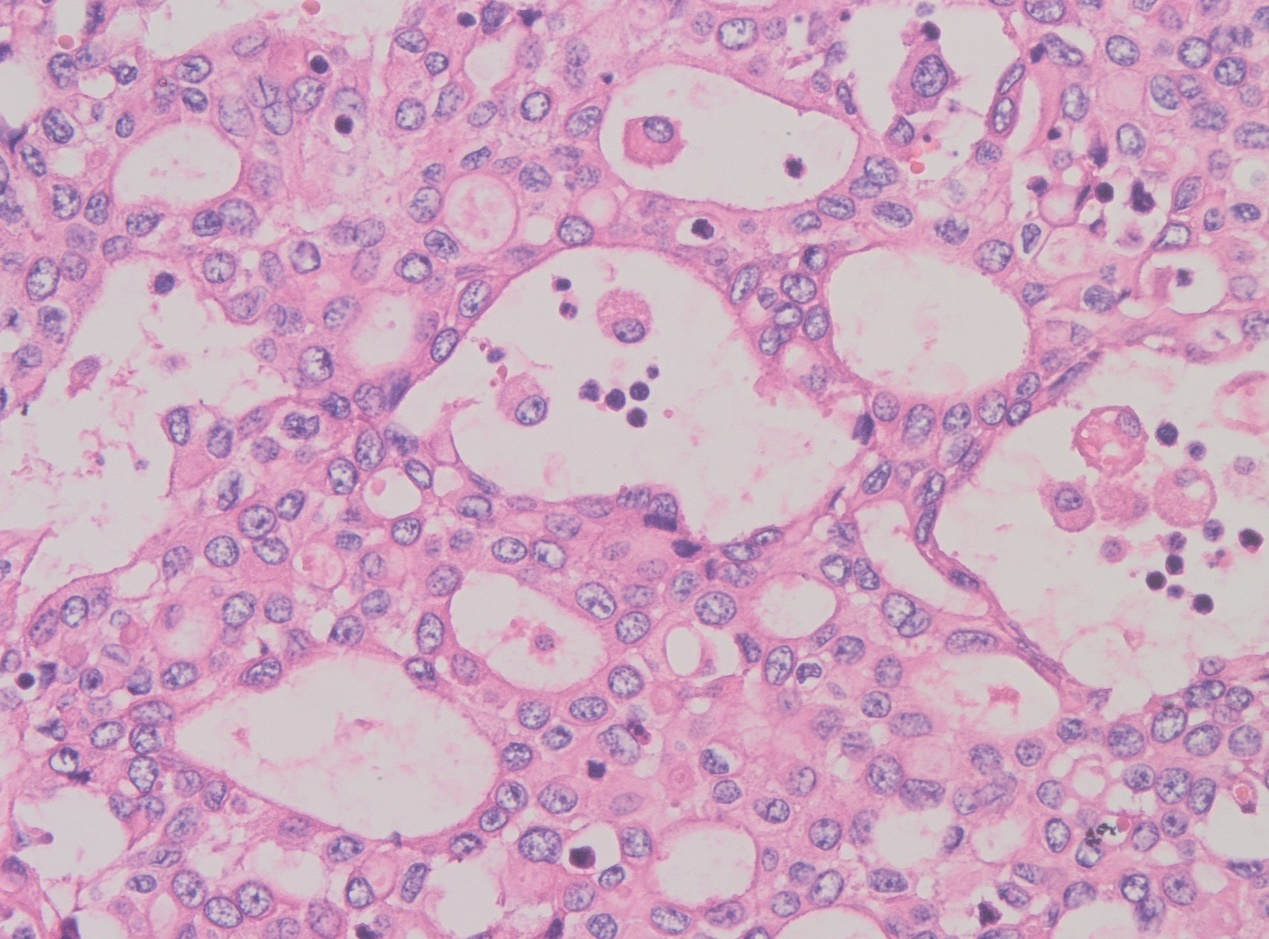
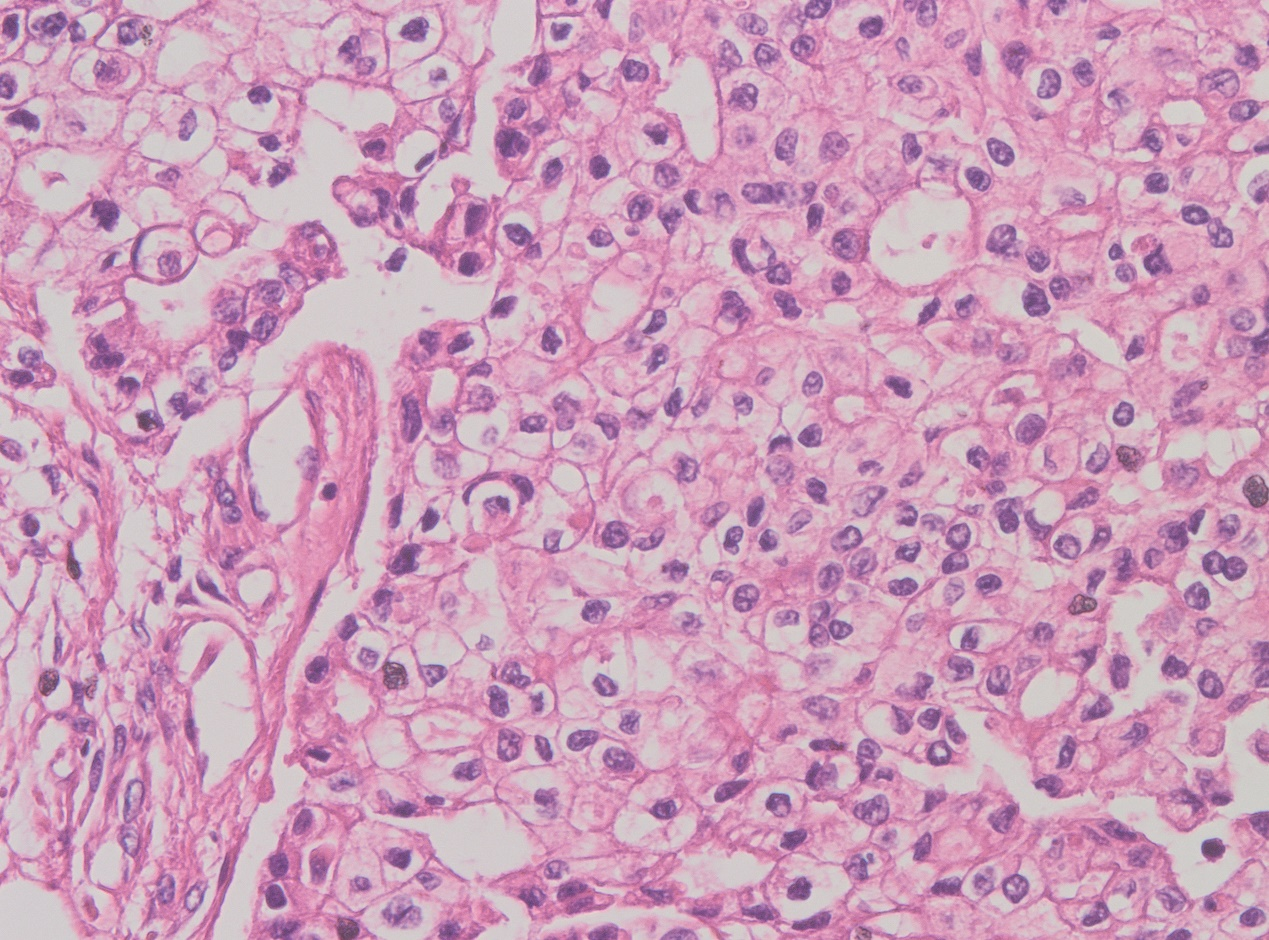
高倍镜下,肿瘤细胞胞浆较丰富,嗜酸性细颗粒状,细胞核大小较一致,略呈空泡状,部分细胞核可见位于中央的小核仁。
免疫组化特征:α1抗胰蛋白酶(+),CK8/18(+),Syn(灶+),CD56(灶+),CgA(-),CD10(-),β-catenin(膜+),P504S(-),Ki67阳性率约15%。
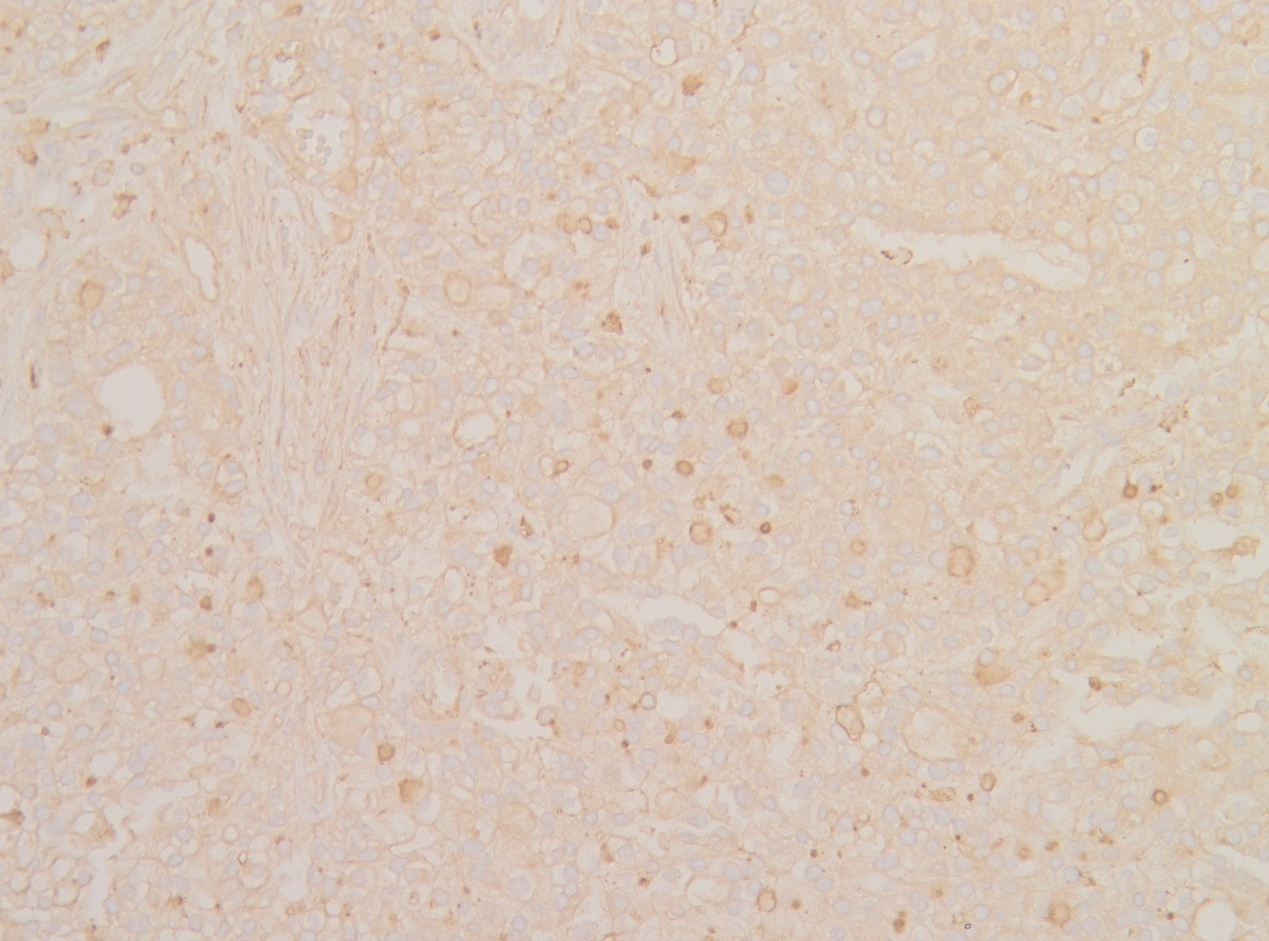
α1抗胰蛋白酶(+)
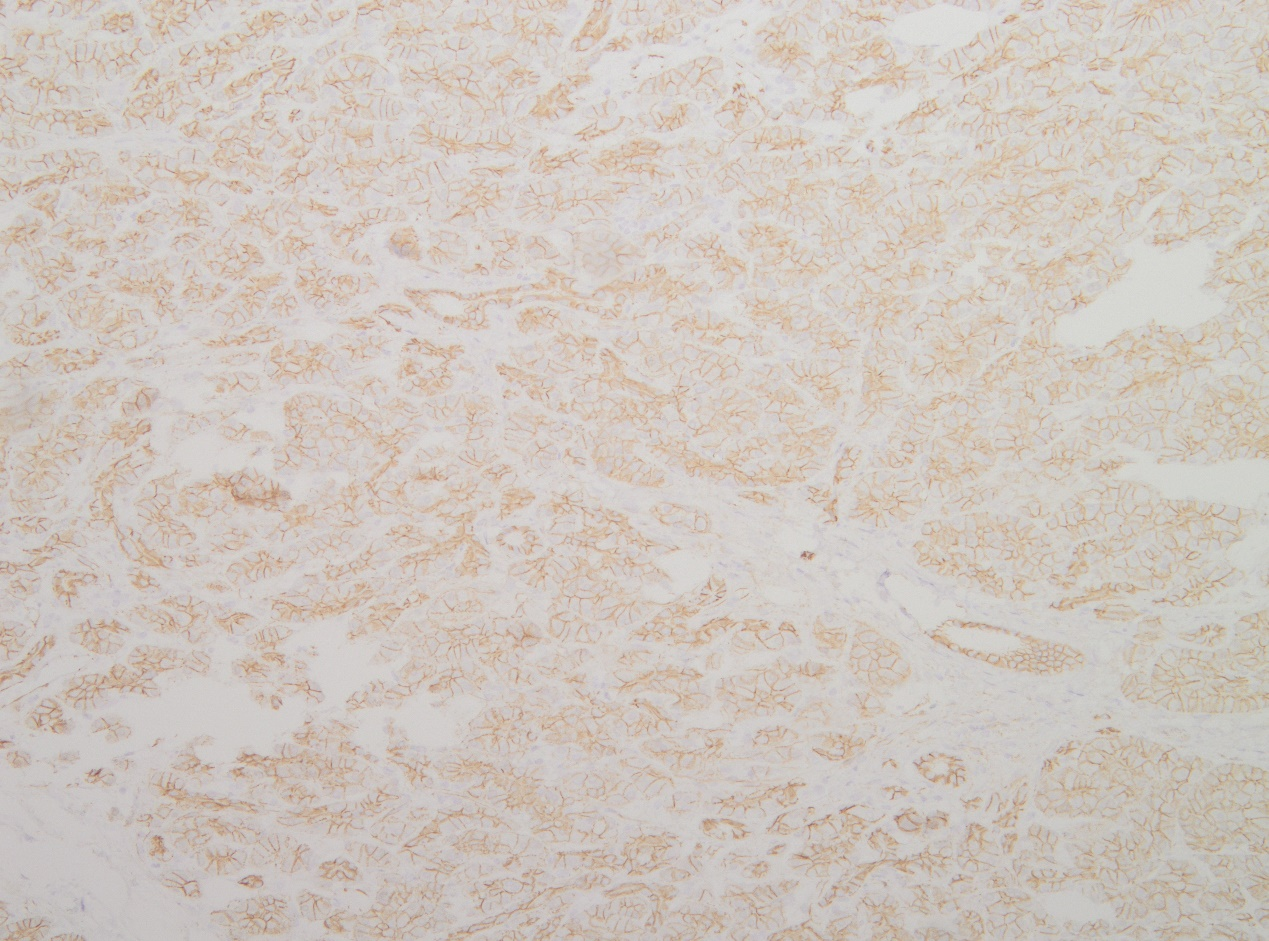
β-catenin(膜+)
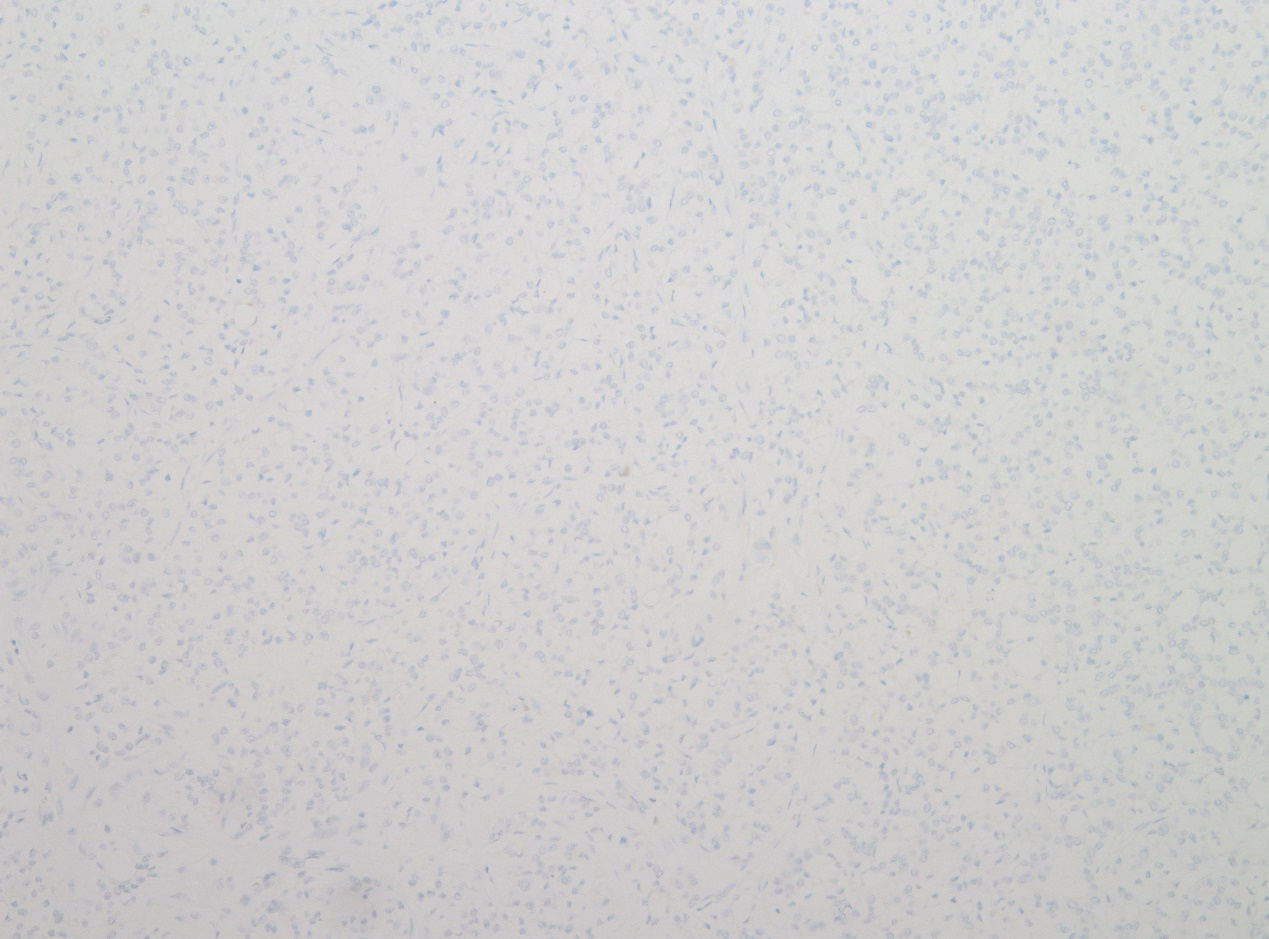
CD10(-)
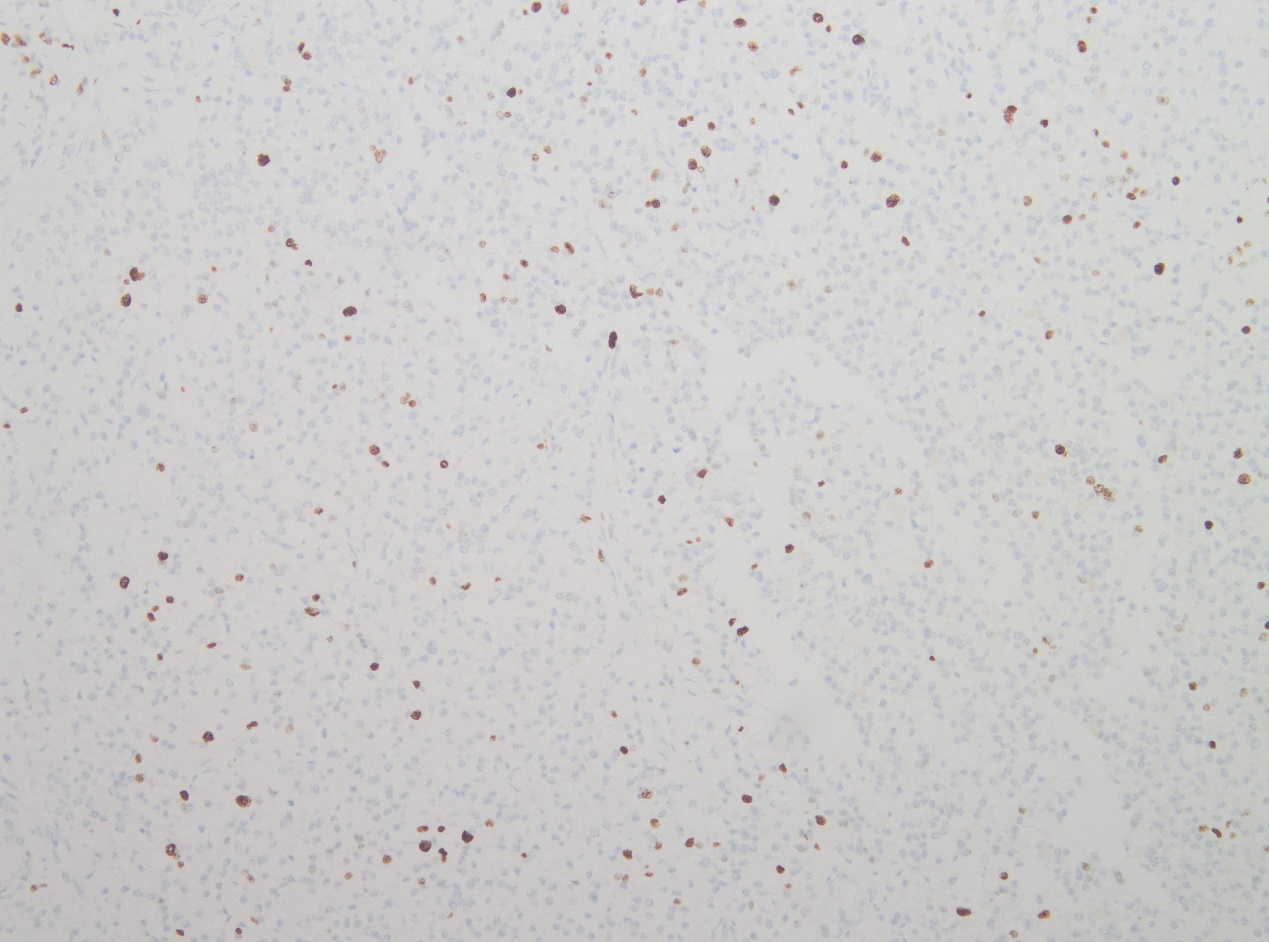
Ki67阳性率约15%
病理诊断:胰腺腺泡细胞癌。
讨论
定义:一种少见的、原发于胰腺的恶性上皮源性肿瘤。
ICD-O编码:8550/3
临床特征:在成人所有胰腺外分泌肿瘤中占比约1%-2%,在儿童所有胰腺外分泌肿瘤中占比约10%,好发于老年人,男性稍多见。临床表现不具特异性,多为腹痛、腹泻、恶心呕吐、体重减轻等消化道症状,肿瘤位于胰头且明显压迫或浸润胆管时可伴有胆道梗阻及黄疸。约10%-15%的患者可出现皮下脂肪坏死、多发关节疼痛等症状,为过多脂肪酶分泌入血所致,手术切除肿物后可获得缓解。
病理形态
1.大体特征:大多单发,体积常较大,平均直径10cm,圆形或多结节状,膨胀性生长,肉眼观边界尚清。颜色灰白至红棕,质地较软,可伴坏死及囊性变,常侵犯临近组织。
2.镜下特征
低倍镜下肿瘤常被纤维条索分割成大结节状,结节内血管丰富,可伴坏死,促纤维化间质不明显。肿瘤细胞可排列呈梁索状、腺泡状、筛状、腺样、实性等多种生长方式。
肿瘤细胞胞浆量中等,嗜酸或嫌色,可见细小的胞质内颗粒,为肿瘤细胞内的酶原颗粒。细胞核圆形或卵圆形,可见单个居中核仁,通常异型性不明显,核分裂象多少不一,平均为14/10HPF。
腺泡细胞癌中可含有向导管及神经内分泌细胞分化的成分,当每种成分超过30%时称混合性腺泡-导管癌或混合性腺泡-神经内分泌癌。
3.免疫组化:α1抗胰蛋白酶、胰蛋白酶、糜蛋白酶、脂肪酶可呈阳性,上皮标记物如AE1/AE3、CK8/18、CAM5.2等可呈阳性。Ki67通常较高,平均约30%。Syn、CgA可灶阳,若超过30%则应诊断为混合性腺泡-神经内分泌癌。
分子遗传学特征:大约半数腺泡细胞癌存在11p染色体的杂合性缺失,约四分之一存在APC/β-catenin信号通路异常。
预后:属高度侵袭性肿瘤,预后差,确诊后平均生存时间约18个月,年长者及肿瘤较大者预后较年轻者及肿瘤较小者差。超过半数的患者确诊时已经发生转移,多转移至淋巴结、肝、肺及腹膜。
鉴别诊断:
1.神经内分泌肿瘤:当腺泡细胞癌呈巢状、梁状或脑回状生长方式,并且核异型性较小时容易与神经内分泌癌混淆。但腺泡细胞癌比神经内分泌肿瘤更易见核分裂象及核仁,而神经内分泌肿瘤则表现为胡椒盐样核。神经内分泌肿瘤表达神经内分泌标记物Syn、CgA、CD56、INSM1。
2.实性假乳头状肿瘤:肿瘤细胞粘附性差,远离血管的肿瘤细胞常常脱落,从而形成假乳头状外观,没有真正的腺管形成。细胞核圆形或卵圆形,染色质细腻,可有核沟。免疫组化表达CD10、PR、vimentin,β-catenin核阳性。
3.胰母细胞瘤:罕见,发生于婴幼儿,多为边界清楚的细胞巢,常见纤维分隔,主要由不同分化阶段的腺泡细胞组成,可有少量导管或内分泌分化。鳞状细胞巢的形成是胰母细胞瘤的特点之一。胰酶免疫组化标记阳性。
4.导管腺癌:常呈腺管状生长方式,浸润性而非膨胀性生长,与周围组织界不清,具有特征性的癌性间质,表现为少血管的纤维胶原样。常可见神经侵犯,胞浆内可见黏液。
参考文献
1.临床病理诊断与鉴别诊断——肝、胆、胰疾病.丛文铭、郑建明主编.
2.WHO Classification of Tumours 5th Edition. Digestive System Tumours. Edited by WHO Classification of Tumours Editorial Board.
3. Calimano-Ramirez LF, Daoud T, Gopireddy DR, Morani AC, Waters R, Gumus K, Klekers AR, Bhosale PR, Virarkar MK. Pancreatic acinar cell carcinoma: A comprehensive review. World J Gastroenterol. 2022 Oct 28;28(40):5827-5844.
4. Xing-Mao Z, Hong-Juan Z, Qing L, Qiang H. Pancreatic acinar cell carcinoma-case report and literature review. BMC Cancer. 2018 Nov 8;18(1):1083.
5. Al-Hader A, Al-Rohil RN, Han H, Von Hoff D. Pancreatic acinar cell carcinoma: A review on molecular profiling of patient tumors. World J Gastroenterol. 2017 Dec 7;23(45):7945-7951.




 苏公网安备 32011402010112号
苏公网安备 32011402010112号