女,45岁,于1个月前出现阴道的异常出血,伴腹部疼痛。就医后发现宫颈赘生物,行病理活检。
大体所见:灰白不整组织一块,体积:3.4cm×2.1cm×2cm。
镜下形态:低倍镜腺体呈分叶状排列,腺体细胞具有轻-中度异型性,细胞形状不规则、胞质明显嗜酸、核明显增大;间质成分直接聚集于上皮周围(所谓“生发层”),细胞呈套袖状生长,细胞密度增高,轻度异型性。
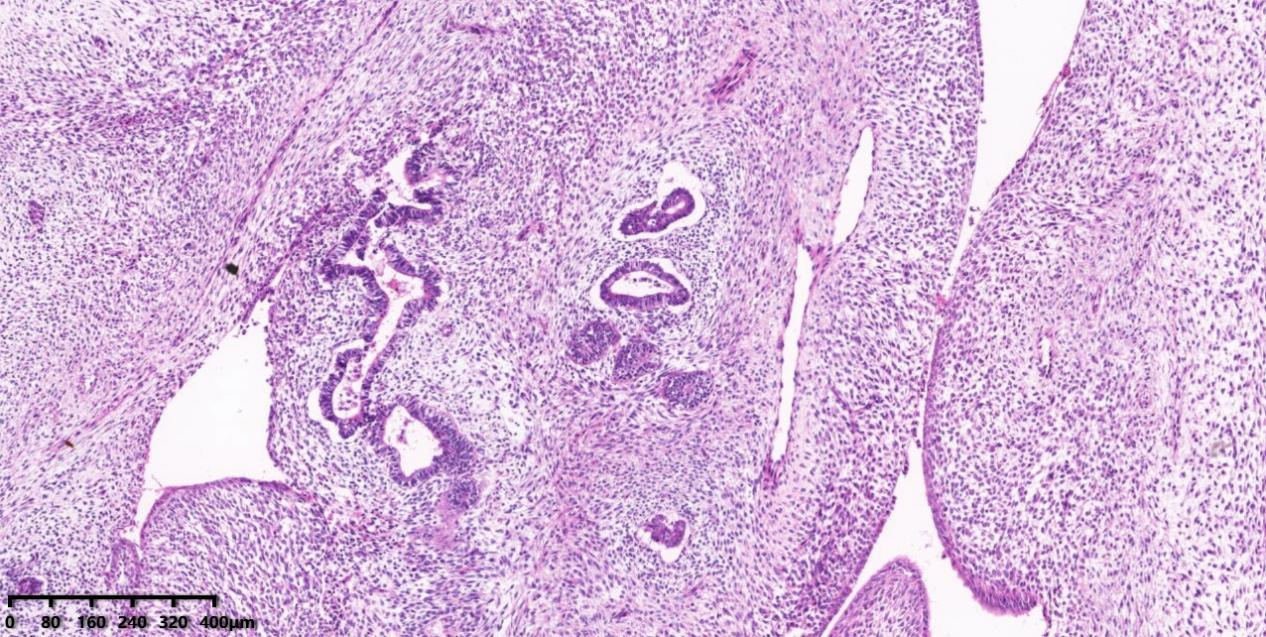
图1、低倍镜下可见分叶状腺体周围间质细胞排列密集,形成“生发层”结构。
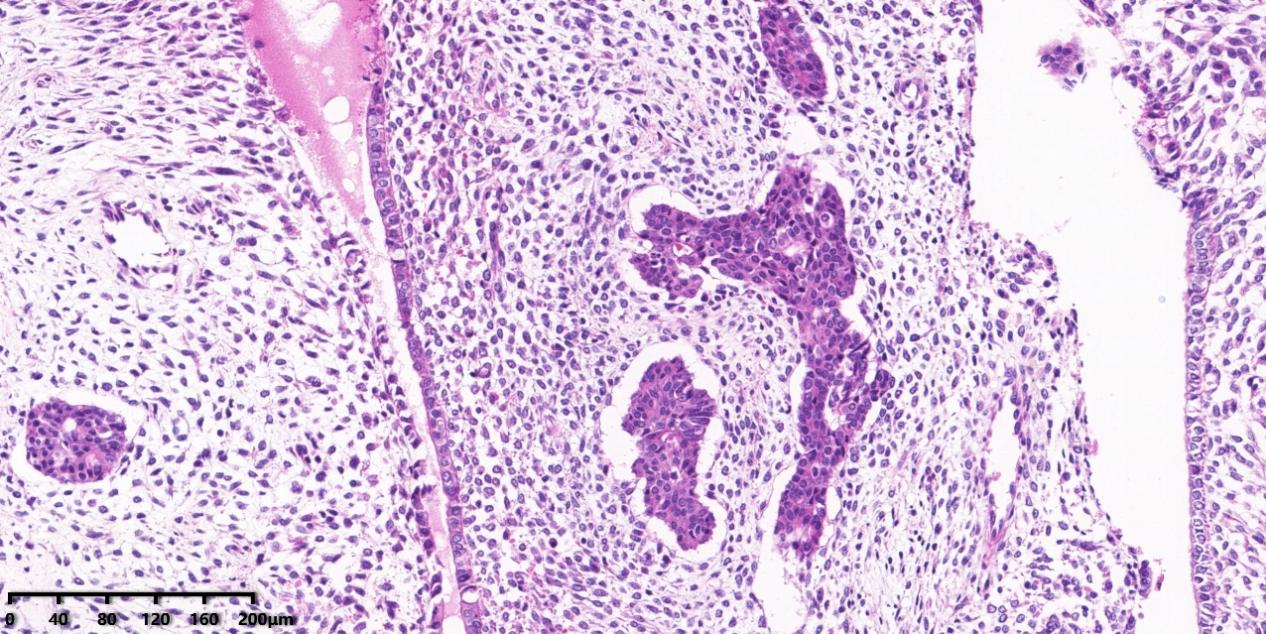
图2、中倍镜可见腺体常均匀分布, 部分呈叶状或囊状外观。
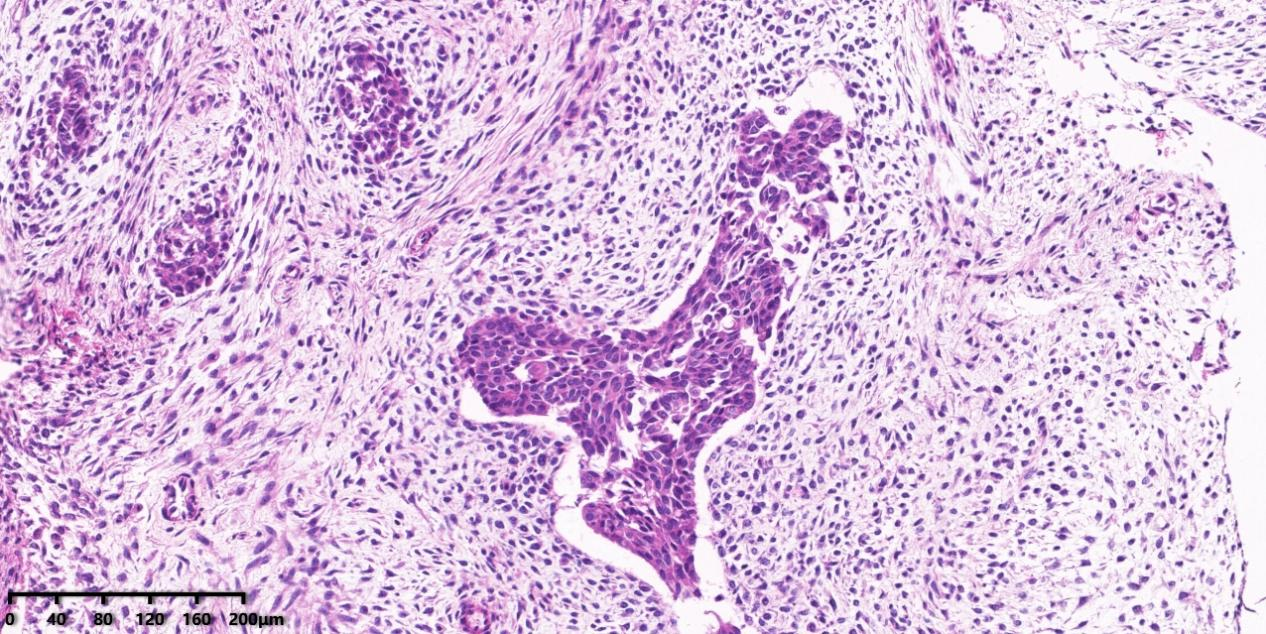
图3、中倍镜下可见腺体及间质细胞丰富,具有轻度异型性。
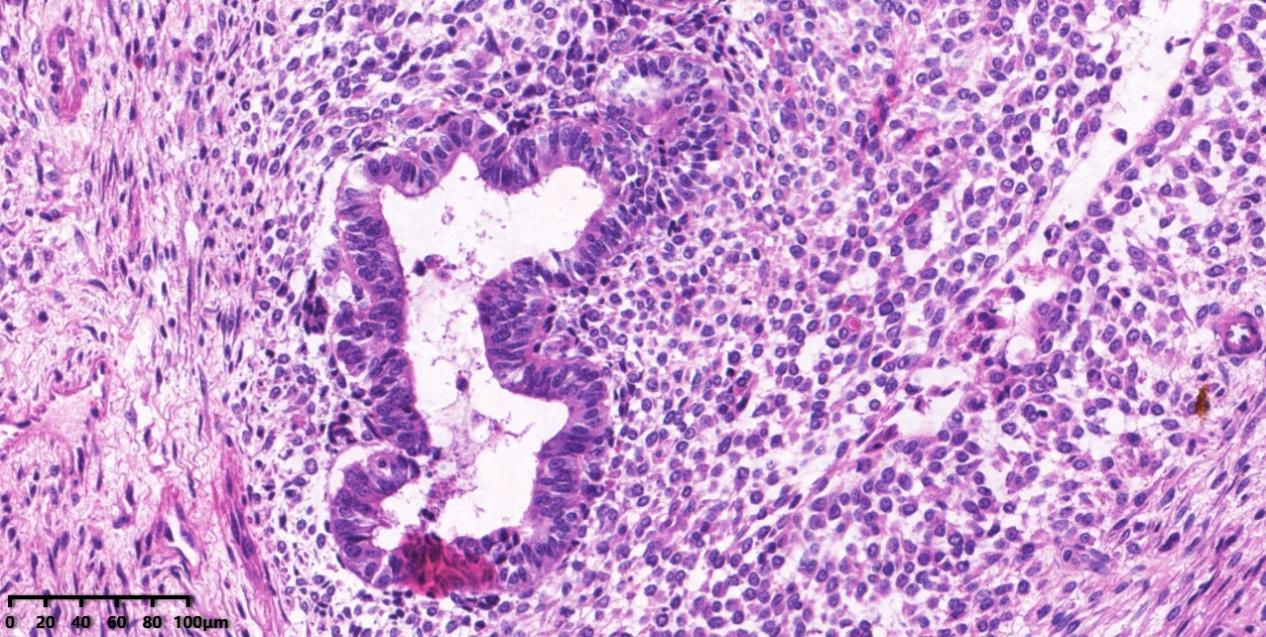
图4、高倍镜下可见腺体具有中度异型性,细胞形状不规则、胞质明显嗜酸、核明显增大;间质细胞核增大,深染,可见小核仁及病理性核分裂象。
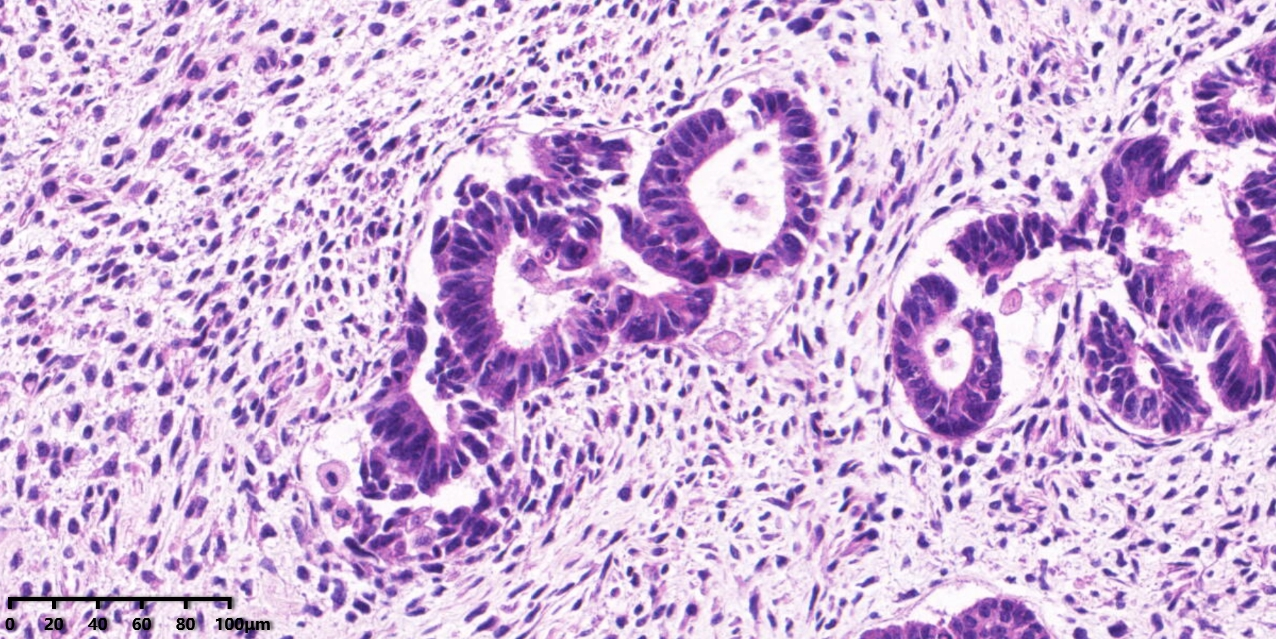
图5、高倍镜下可见间质细胞核增大,胞浆嗜酸性,略偏位,横纹肌样形态。
免疫组化结果:梭形细胞呈ER(+),PR(+),SMA(+),CD10(+),H-cald(-),Desmin(-),P16(+),P53(野生型),Ki-67(+,约10%)。
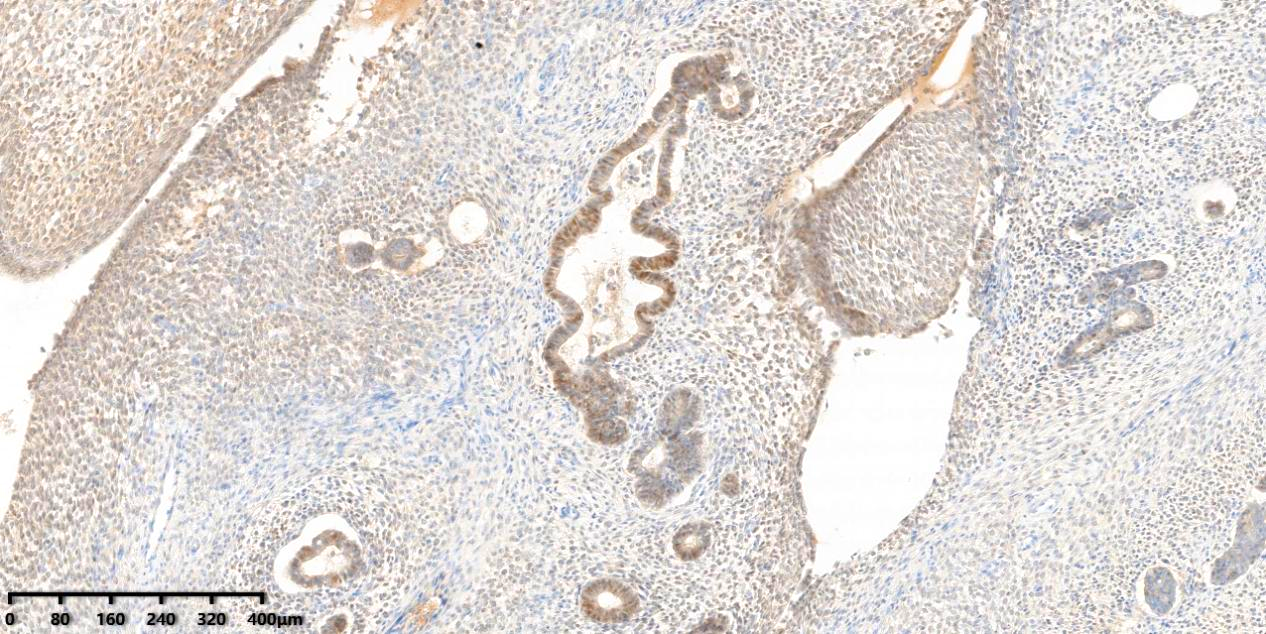
图6、免疫组化显示腺体及间质细胞ER均阳性表达。
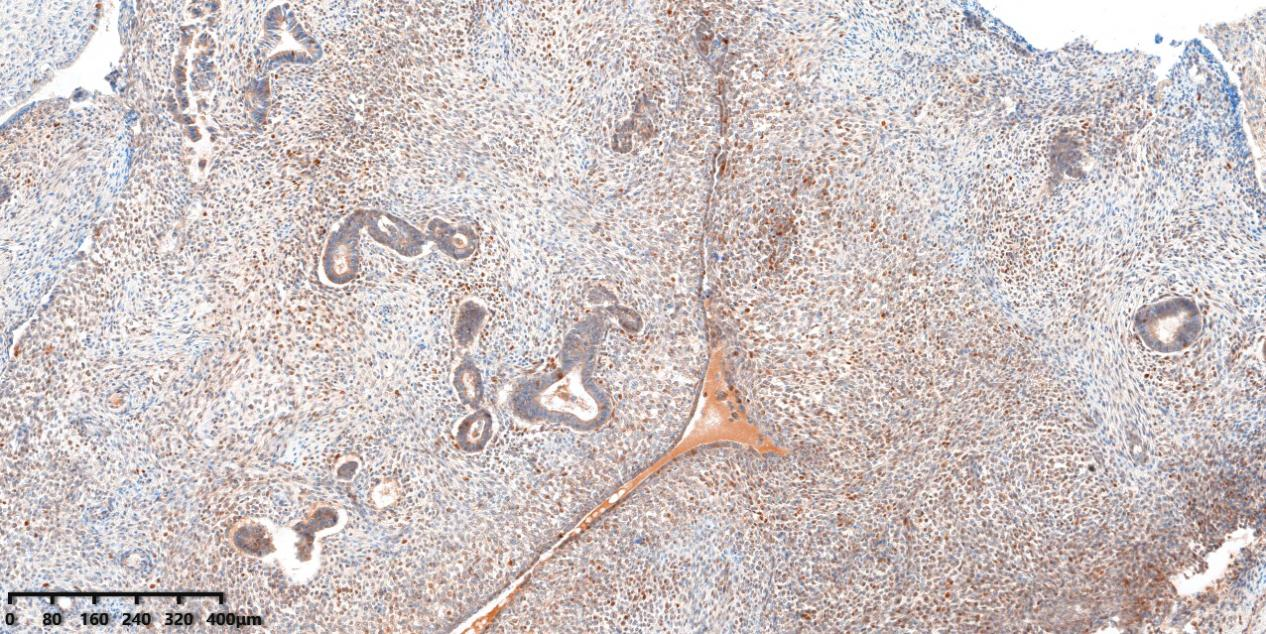
图7、免疫组化显示间质细胞CD10阳性。
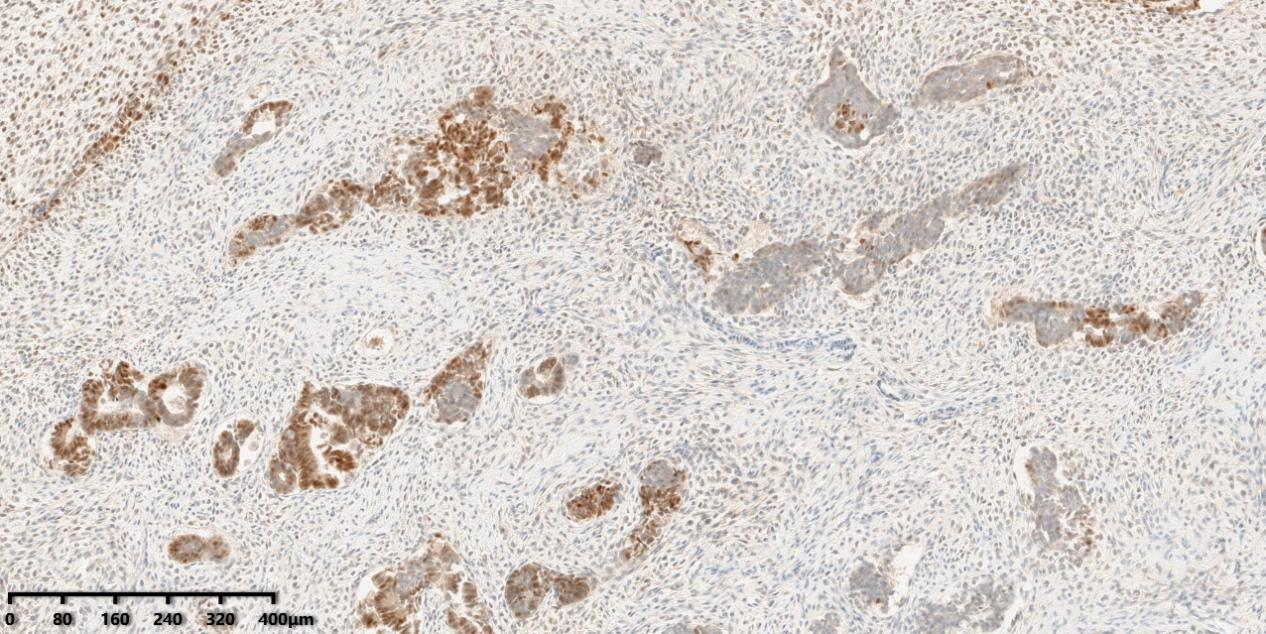
图8、免疫组化显示腺体及间质细胞PR均阳性表达。
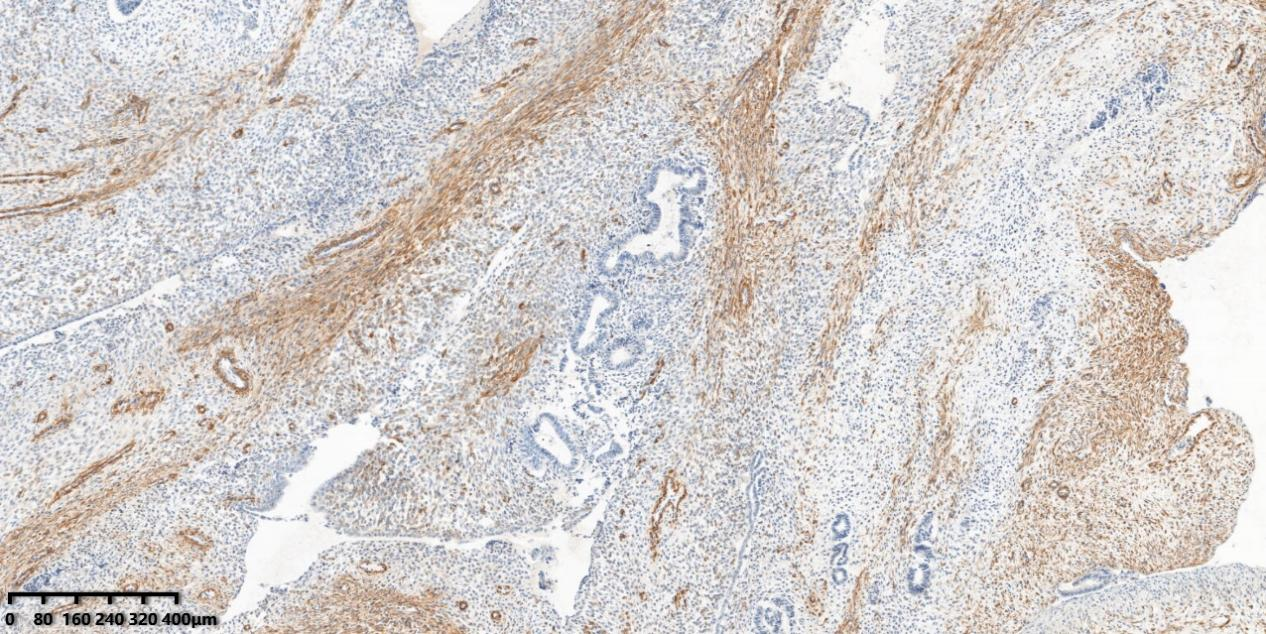
图9、免疫组化显示间质细胞SMA阳性表达。
病理诊断:宫颈低级别腺肉瘤。
注:有学者认为既往被诊断的“腺纤维瘤”很可能就是分化良好、核分裂象少的腺肉瘤。若因仅凭核分裂象稀少而诊断为腺纤维瘤时,可能会出现肿瘤复发且预后不良。因此即使核分裂活性较低,但在低倍镜下发现典型的肿瘤结构时,也应该诊断为腺肉瘤。
讨论
宫颈腺肉瘤(Adenosarcoma of the uterine cervix)的定义是由良性轻度非典型的苗勒上皮腺体和低级别恶性间质成分的混合性双相肿瘤。其发病机制可能源自既往存在的子宫内膜异位,发生与HPV感染无关。发病十分罕见,约占女性生殖形态腺肉瘤的2%。罕见宫颈内多灶性病变、同时累及宫颈和子宫体。【临床特征】
多在绝经后,患者平均年龄31-38岁之间。 常表现为阴道出血,有“复发性息肉”病史。
【大体检查】
肿瘤呈分叶状、息肉状,常见裂隙;或切面呈囊性。
【组织学特征】
腺体为良性,具有轻度异型性的苗勒上皮腺体,常均匀分布,部分呈叶状或囊状外观,常被覆宫颈型上皮,可伴鳞化,偶见输卵管型/子宫内膜样腺体,几乎所有病例均可见到局灶上皮细胞的非典型性,表现为形状不规则、胞质明显嗜酸、核增大,但都不足以诊断为恶性。
间质常为低级别,伴有多少不等的核分裂象(诊断标准:≥4个/10HPFs),常聚集在腺体周围,形成“袖套状生发层”(Cambium layer),向腔内呈息肉样突起,形成“叶状结构”,同源性间质成分包括子宫内膜间质肉瘤、纤维肉瘤及平滑肌肉瘤,1/4病例可有异源性间质成分:胎儿型软骨、横纹肌母细胞(更常见)或脂母细胞。高级别肉瘤成分至少占肿瘤的25%,在低倍镜下即可识别的多形性肉瘤细胞:细胞核增大,深染,核仁明显,常见横纹肌肉瘤分化,也可发生性索分化。
【鉴别诊断】
(1)腺纤维瘤
与分化好的腺肉瘤难以鉴别,属于Müllerian混合性肿瘤(混合性上皮-间叶肿瘤):上皮为各型Müllerian上皮,间叶为成熟纤维性间质。
(2)梭形鳞状细胞癌:偶尔围绕腺体分布形成袖套样外观,p63、AE1/AE3阳性,CD10阴性可帮助鉴别。
(3)子宫体腺肉瘤突入宫颈时需要与子宫腺肉瘤进行鉴别诊断,子宫腺肉瘤70%发生于宫体,鉴别必须依靠充分、明确的大体取材,子宫切除标本,细致的分段诊刮标本。
(4)宫颈葡萄状横纹肌肉瘤:呈宽乳头状、分叶状,位于黏膜下,表面黏膜可完整、糜烂、溃疡、或发生鳞状上皮化生,特征性形态:“生发层”(cambium layer)——紧邻黏膜上皮的下方,深染密集的肿瘤细胞形成宽带状区域,数层至十数层。生发层下方间质疏松、黏液水肿样,内有散在的分化程度不等的横纹肌母细胞。免疫组化Desmin、MyoD1、Myogenin阳性。
(5)子宫内膜间质肉瘤:较少发生于宫颈,且通常含有上皮样或性索样成分,周边可见良性腺体,而腺肉瘤中的腺体呈广泛分布,可见叶状结构,周围间质特征性地呈套袖样生长。
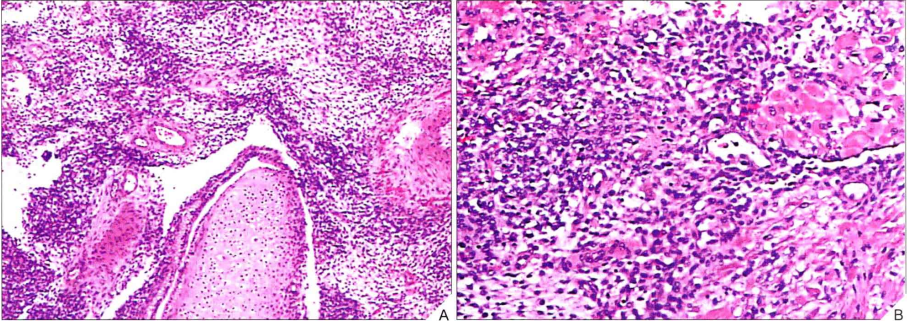
图7:A,宫颈腺肉瘤伴有异源性软骨成分;B,宫颈腺肉瘤伴横纹肌分化。
【免疫组化】
上皮成分CK阳性,ER和PR通常阳性。腺肉瘤中的间叶细胞通常显示CD10胞质阳性,ER 、PR及WT-1核阳性。
【治疗与预后】
腺肉瘤的治疗主要为全子宫及双侧输卵管和卵巢切除术。宫颈腺肉瘤的复发率约25%-40%, 死亡率约10 % - 24 %。与预后密切相关的因素:① 子宫外扩散;② 深肌层浸润,超过肌层1/2;③ 肉瘤成分过度生长;④ 脉管内可见肿瘤细胞,⑤ 伴有异源性成分。
参考文献
[1] Amant F, Steenkiste E, Schurmans K, et al. Immunohistochemical expression of CD10 antigen in uterine adenosarcoma. Int J Gynecol Cancer. 2004 Nov-Dec;14(6):1118-21.
[2] McCluggage WG. Mullerian adenosarcoma of the female genital tract. Adv Anat Pathol. 2010 Mar;17(2):122-9.
[3] Mohammadizadeh F, Rajabi P, Behnamfar F, et al. Extensive Overgrowth of Sex Cord-Like Differentiation in Uterine Mullerian Adenosarcoma: A Rare and Challenging Entity. Int J Gynecol Pathol. 2016 Mar;35(2):153-61.




 苏公网安备 32011402010112号
苏公网安备 32011402010112号