非小细胞肺癌(NSCLC)是世界上最常见的恶性肿瘤之一,近年来免疫检查点抑制剂成为癌症治疗的热点之一。在2020年美国临床肿瘤学会(ASCO)年会上,涉及到肿瘤免疫治疗相关的生物标记物的一些研究。91360特邀苏州大学附属第一医院病理科郭凌川教授对今年ASCO上NSCLC中免疫治疗相关的生物标志物最新进展进行梳理。

一、PD-L1表达与免疫治疗疗效的关系
郭凌川教授:[摘要9500] 3期CheckMate 227第一部分研究发现,对于晚期NSCLC和肿瘤PD-L1表达≥1%(初步分析)或<1%(预先指定的描述性分析)的初治病人,NIVO+IPI 作为一线治疗比化疗明显提高总生存(OS)。本次会议上更新了最少3年的随访结果。
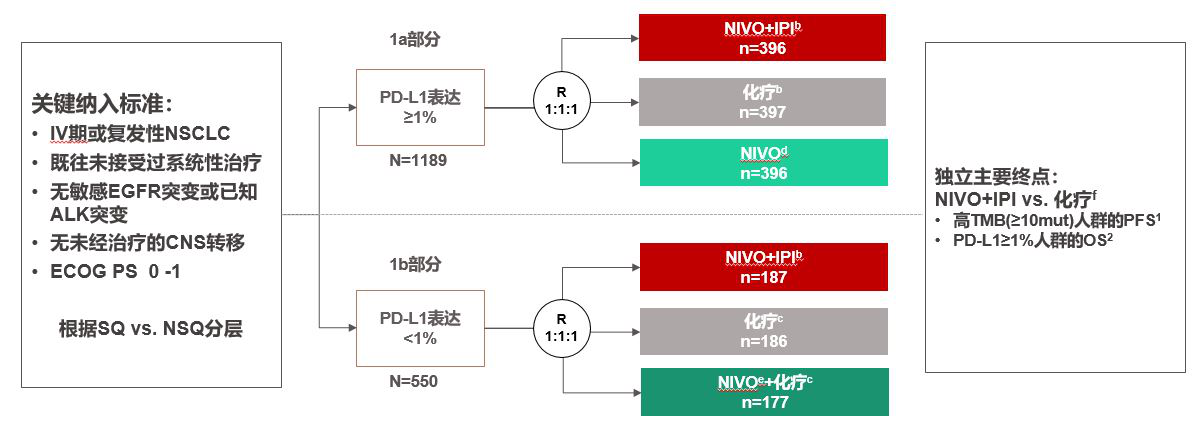
疗效分析显示,PD-L1≥1%的患者继续从NIVO+IPI获益,与化疗相比OS延长(HR:0.79;95%CI,0.67-0.93);3-y OS率分别为33%(NIVO+IPI)、29%(NIVO)和22%(化疗)。
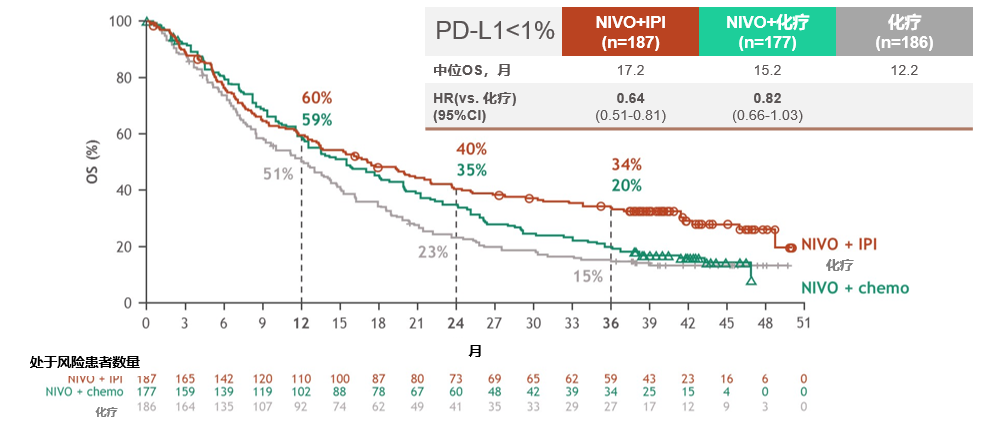
在PD-L1<1%的患者中,NIVO+IPI与化疗的OS HR分别为0.64(95%CI,0.51~0.81),3-yOS率分别为34%(NIVO+IPI),20%(NIVO+化疗)和15%(化疗)。
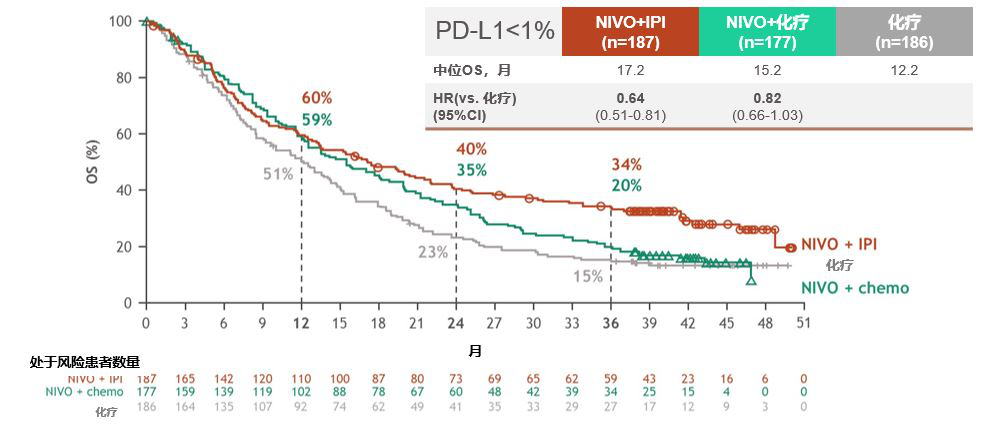
结果表明,与化疗相比,NIVO+IPI作为一线对晚期NSCLC的患者提供持久和长期的OS获益。
郭凌川教授:[摘要9501] IV期/复发NSCLC一线NIV+IPI+2周期化疗 vs 4周期化疗:CheckMate 9LA 研究对主要研究终点总生存期(OS)的预设期中分析结果显示,随访最少8.1个月,与单用化疗相比,欧狄沃联合伊匹木单抗及两个周期化疗能够使患者的死亡风险降低31% [HR:0.69]。此外,在更长的随访期(最少12.7个月),与单用化疗相比,该联合治疗方式能够为患者带来持续的OS获益(中位OS:15.6个月vs 10.9个月, [HR 0.66])。在亚组分析中,无论患者PD-L1表达水平和肿瘤组织学类型(鳞癌或非鳞癌)如何,所有疗效评估均显示出临床获益。
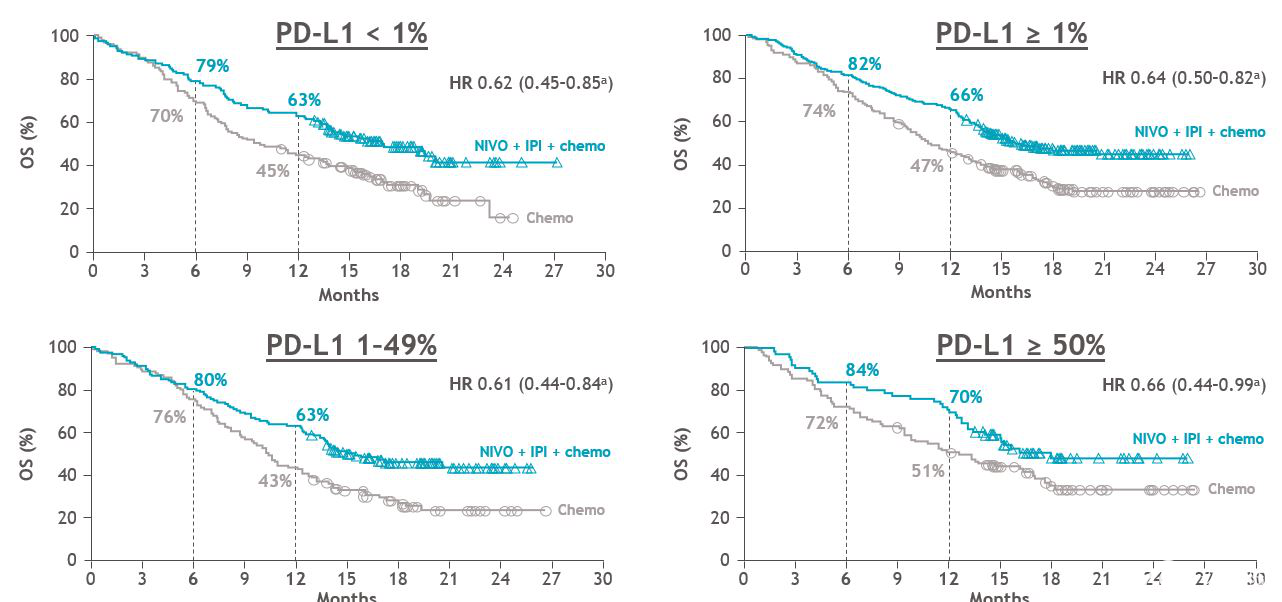
郭凌川教授:[摘要9502] 晚期NSCLC的一线治疗包括PD-1检查点抑制剂(ICI)单药治疗,以及联合化疗。与化疗相比,联合ICI也证实有更好的生存。研究比较标准化疗联合双免疫检查点抑制剂方案和双免疫检查点抑制剂方案在晚期NSCLC一线治疗中的疗效。试验组采用标准化疗联合双免疫检查点抑制剂(Durvalumab+Tremelimumab)→Durv±培美曲塞(非鳞)维持。对照组选用D+T方案。主要研究终点OS,次要研究终点包括PFS、ORR、安全性。最终有301名患者入组,在中位随访16.6个月后,该项研究未能达到主要研究终点。在预先计划的亚组中,不同TMB(以20mut/Mb为界)和不同PD-L1表达水平亚组中化疗+D+T方案同样也未能展现出明显的OS获益。仅在TPS≥50%人群,化疗+D+T有OS获益趋势(HR 0.64, 95% CI 0.40-1.04, p=0.07)。
郭凌川教授:[摘要 9503] CITYSCAPE是一项抗TIGIT抗体加Atezo与安慰剂加Atezo作为一线治疗PD-L1 表达的NSCLC随机、双盲、II期研究的初步研究。研究要求入组患者PD-L1 TPS≥1%。主要研究终点是ORR和PFS,次要终点是DOR、OS和安全性。探索性终点是PD-L1状态对ORR和PFS的影响。
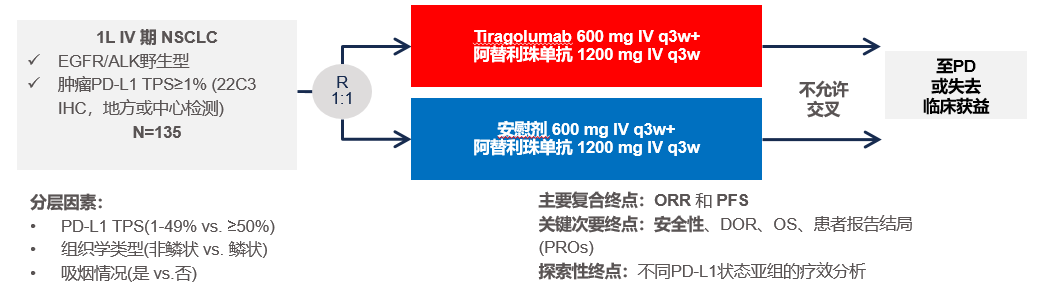
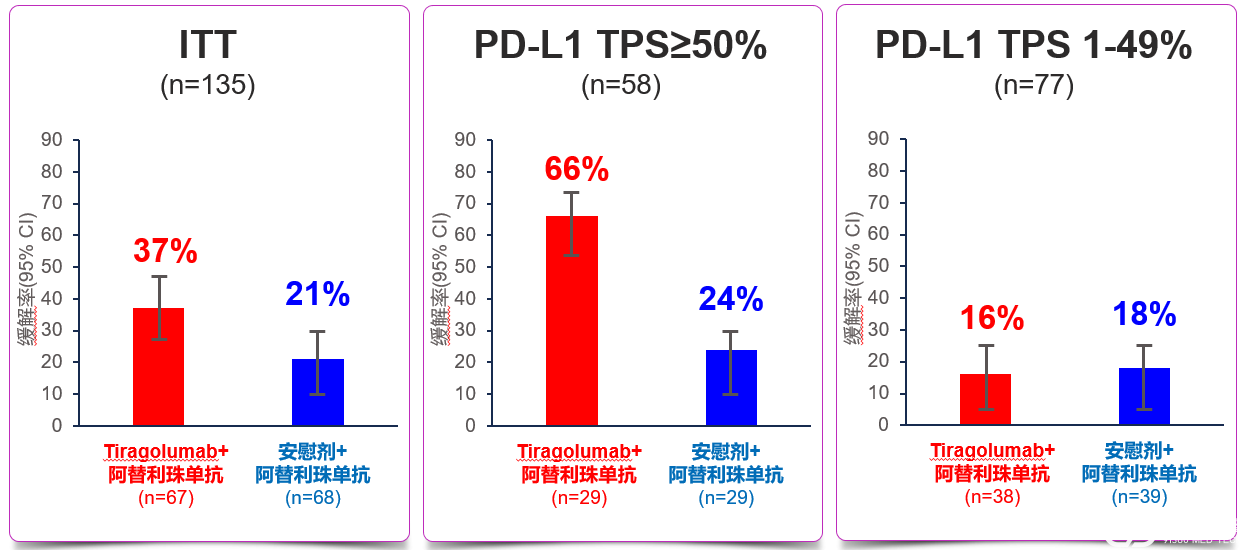
疗效分析显示,在中位随访10.9个月后,Tira+Atezo组在ORR和PFS上有明显提高,TPS≥50%患者获益更多。
郭凌川教授:[摘要9539] 本研究是评估PD-L1 TPS作为预测鳞癌(SQ)和非鳞癌(NSQ)NSCLC患者接受一线Pembrolizumab(P)后总生存期(OS)的差异价值。研究的主要终点是TPS≥50%与TPS<50%相比,第一剂量Pembrolizumab的总存活率(OS)。研究结果发现在NSQ患者中,TPS≥50%的OS明显长于TPS<50%,HR为0.71(95%CI:0.53-0.94;p=0.018)。在SQ患者中,TPS≥50%与TPS<50%和较长的OS无关,HR为0.89(95%CI:0.64-1.25;p=0.514)。该项研究提示PD-L1可能不是肺鳞状细胞癌中使用检查点抑制剂的一种合适的预测生物标志物。
二、NSCLC中免疫治疗相关的血液生物标志物
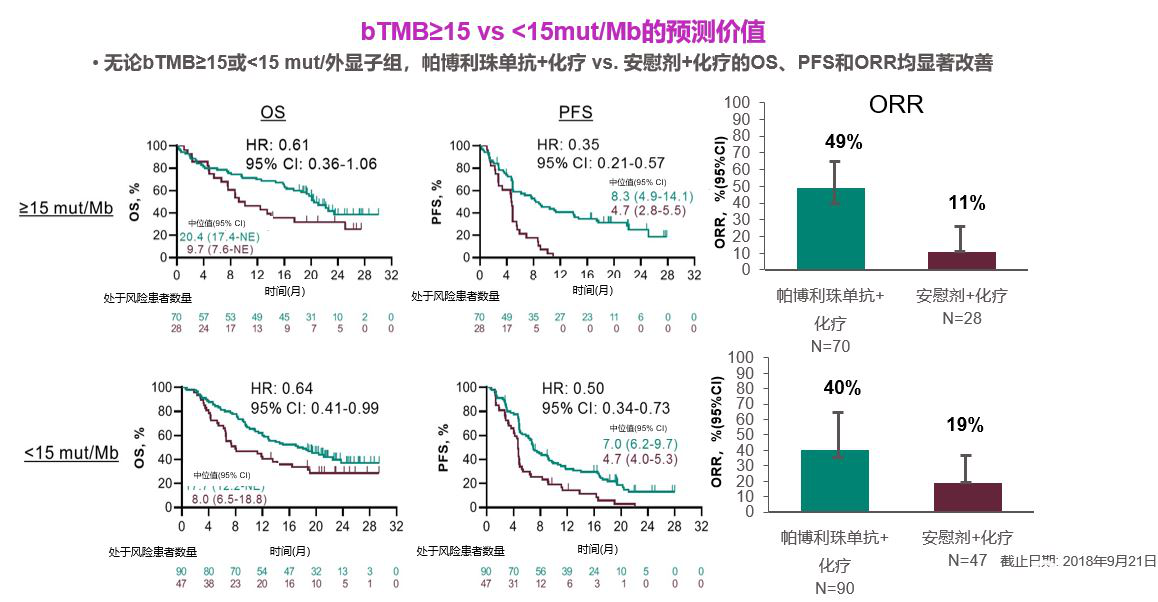
郭凌川教授:[摘要9521] 在Keynote-189试验中,研究者发现通过全外显子组测序评估的组织TMB(tTMB)与免疫治疗疗效没有显著相关性,但在tTMB≥175和tTMB<175mut/exome亚组中,pembro+化疗比安慰剂+化疗改善了结果。研究者继续探索bTMB与免疫治疗疗效的关联。将616例患者随机分为2:1化疗组和安慰剂+化疗组。使用Guardant Health Omni试验评估cfDNA中的bTMB。研究发现bTMB作为连续变量与Pembro+化疗组或安慰剂+化疗组的OS或ORR无显著关联;bTMB与Pembro+化疗组的PFS显著相关,但与安慰剂+化疗组的PFS无显著相关性。bTMB和tTMB评分呈中度相关(r=0.61)。与先前基于tTMB的研究结果相似,bTMB在Pembro+培美曲塞和顺铂作为肺癌一线治疗的临床疗效预测作用有限。
郭凌川教授:[摘要 9523] 最近的数据显示,肿瘤抑制基因ARID1A与较高的抗肿瘤免疫力相关,可作为预测NSCLC中免疫检查点治疗疗效的生物标志物。该项研究使用液体活检查方法检测了大量晚期NSCLC患者ctDNA中检测到的ARID1A改变,并探讨了ARID1A与肺癌驱动因素改变和其他免疫检查点抑制剂生物标记物的相关性。结果显示与腺癌相比,鳞状癌中fARID1A突变明显更常见(5.1% vs 3.8%,p=0.0007)。在fARID1A突变患者中,EGFR外显子19缺失突变显著减少(4.9% vs 11.1%;p<0.0001),EGFR L858R突变显著减少(4.0% vs 7.0%;p<0.0001),而BRAF V600E突变显著增多(2.2% vs 1.4%;p=0.0338)。伴和不伴有fARID1A突变的患者ALK和ROS1融合频率及STK11突变频率无显著性差异(8.0% vs 6.8%;p=0.126)。在fARID1A突变患者中,KRAS突变的频率明显更高(31.1% vs19.4%;p<0.0001)。研究显示 fARID1A与多个肺癌驱动因素改变频率的显著差异有关,尤其与EGFR突变显著相关,而与STK11突变的频率未见明显相关性。KRAS突变在fARID1A突变患者中更常见,最近的数据显示,KRAS突变,特别是KRAS G12C,可能是非小细胞肺癌ICPi反应的有利预测因子。
郭凌川教授:[摘要 9545] 该研究为一项基于血液的宿主免疫图谱在进展期NSCLC一线免疫治疗中真实世界的研究,目的是评估经临床验证的、基于血液的宿主免疫分类器(HIC)预测ICI治疗结果的能力。所有入选的患者在开始治疗前都要接受测试并指定为HIC-热(HIC-H)或HIC-冷(HIC-C)。研究结果显示在包括ICI在内的多种方案中,HIC-H患者比HIC-C患者存活时间更长,HIC结果与PD-L1评分无关(p=0.81)。该项研究结果表明,基于血液的宿主免疫分析可能为选择两种常见ICI方案的非小细胞肺癌患者提供有临床意义的信息,该方案独立于PD-L1评分,并与PD-L1评分相辅相成。
郭凌川教授:[摘要 9561] 研究结果显示在进展期NSCLC患者中,高基线血浆可溶性BTN2A1浓度与ICI疗效的改善相关,但与化疗结果无关,提示基线可溶性BTN2A1水平是ICI疗效的潜在预测生物标志物。
三、NSCLC中免疫治疗其他生物标记物探索
郭凌川教授:[摘要 9530] SWI/SNF染色质重塑复合物被报道参与免疫检查点抑制剂(ICI)的敏感性和抵抗力。然而,它们在非小细胞肺癌(NSCLC)中的作用仍不清楚。该项研究分析了SWI/SNF复合体突变与非小细胞肺癌患者ICI临床疗效的关系。在LC-SCRUM-IBIS中1017例NSCLC中有350患者接受了WES检测,显示28%的NSCLC患者存在至少一个SWI/SNF复合体亚基突变。在接受PD-1/PD-L1抑制剂治疗的101例NSCLC患者中,SMARCA4突变与较低的DCB、较短的中位PFS和OS相关。有ARID1A突变的患者往往比没有突变的患者有更好的临床结果。未发现PD-L1表达与SMARCA4或ARID1A突变显著相关。STK11/KEAP1突变患者PD-L1表达率较低(TPS),与无突变的患者相比,临床预后更差。tTMB状态和临床结果之间没有明显的关联。该研究结果提示SMARCA4和ARID1A突变影响非小细胞肺癌患者ICI的临床疗效。这些发现表明SWI/SNF复合体突变可作为预测非小细胞肺癌患者ICI的生物标志物。
郭凌川教授:[摘要 9577] 一篇关于SWI/SNF与免疫治疗疗效的相关性研究,该研究回顾性评估SMARCA4突变的NSCLC中免疫检查点抑制的临床结果。研究结果显示,在2690例NSCLC患者中,8%(N=211)存在SMARCA4突变。在接受免疫检查点抑制剂治疗非鳞状NSCLC患者中,11%携带SMARCA4突变。研究者观察到SMARCA4wt与SMARCA4mut NSCLC在ORR、 mPFS、mOS方面没有差异。然而,在KRASmut NSCLC中,并发现SMARCA4mut患者的ORR(23.1% vs 0.0%;P=0.02)、mPFS(4.8月vs 1.7月;P<0.001)和mOS显著缩短(15.6个月vs 2.7个月;P,0.001)。当同时存在的STK11突变时,SMARCA4mut对KRAS mut NSCLC免疫治疗结果的有害影响保持不变。研究结果分析显示,SMARCA4基因突变定义了具有独特临床病理特征的NSCLC基因组亚群,并使KRAS mut NSCLC的患者免疫治疗效果更差。
郭凌川教授:[摘要 9536] 肿瘤相关成纤维细胞(CAF)是肿瘤微环境(TME)的重要组成部分,在肿瘤进展中起关键作用。然而,CAFs对免疫治疗反应的影响仍不清楚。该项研究采用TCGA和GEO数据库,评估了1768例NSCLC标本中24种免疫细胞和成纤维细胞的浸润丰度,发现几乎所有免疫细胞/成纤维细胞的IMFR都对预后有利。这种现象被称为“CAFs介导的免疫抵抗模式(CMIRP)”。CD8+T细胞预后不佳,CD8+T细胞/成纤维细胞比值(CFR)是保护性预后因素[n=1588;危险性比(HR),0.66;95%可信区间(CI),0.56~0.78;P,0.001]。多变量分析显示CFR是一个独立的预后生物标志物。TCGA泛癌队列证实了CMIRP在癌症中的广泛存在。研究进一步定义了CFR高和CFR低的子群。CFR高表达富含免疫激活途径,包括T细胞活化、细胞溶解和抗原提呈,而CFR低表达与免疫抑制相关,包括转化生长因子b激活、上皮间质转化和血管生成途径。CFR可作为非小细胞肺癌预后和免疫治疗疗效预测的潜在指标。
小结
郭凌川教授:总之,PD-L1虽然作为免疫治疗疗效的生物标志物仍然发挥重要作用,但其本身仍有一定的局限性。随着新的检测技术发展,一些新的生物标志物被发现,尤其是本次ASCO会议上报道的血液生物标志物以及一些基因改变,都显示出预测免疫治疗疗效的价值,但也需要更多的临床试验来验证。相信在不久的将来,免疫治疗的生物标志物将为免疫治疗在临床上的应用带来美好前景。
NP/IO/4793/06/22/20-06/22/22




 苏公网安备 32011402010112号
苏公网安备 32011402010112号