原发灶不明转移癌(Cancer of Unknown Primary, CUP)是指组织学确诊为转移癌,而各种检测未能明确其原发解剖部位。CUP约占所有恶性肿瘤的5%-10%,目前的治疗手段有限,患者的预后较差。近年来,基因组学的进展提示,大部分CUP患者有一个或以上的临床有意义的治疗靶点,为CUP的治疗带来新思路。免疫治疗是近年来的研究热点,在多个瘤种中取得重大进展,CUP能否从免疫治疗中获益呢?今年ASCO的一项研究采用全面基因组测序(CGP)检测了CUP的肿瘤突变负荷,显示相当一部分CUP患者有较高的肿瘤突变负荷。
CUP的特征概述
原发灶不明转移癌(Cancer of Unknown Primary Site, CUP)是指经组织病理学证实为转移性恶性肿瘤,而通过全面的检查仍不能确定原发肿瘤部位的恶性肿瘤。CUP的发病率约占所有恶性肿瘤的5%-10%。临床表现多样、易播散、具有侵袭性及难以预测的转移模式是CUP的临床特点。大多数患者的预后很差,中位生存期6-9个月,1年生存率约为25%,5年生存率低于10%,对于一般情况较差、多个脏器受累的病人,中位生存期约为1个月,87%的患者在3个月内死亡。大多数的CUP对系统性治疗抗拒,化疗仅仅是姑息治疗的手段。
CUP的治疗现状总结
CUP的治疗可依据肿瘤的转移范围进行个体化治疗。如果是局限性的CUP,应根据最可能的原发灶部位而制定治疗方法。如纵隔CUP推荐的治疗方法根据诊断时患者年龄制定;雌激素受体阳性女性腋窝淋巴结或胸膜转移性腺癌患者,治疗依据乳腺癌的治疗指南;局限性累积腋窝或腹股沟淋巴结转移性鳞癌的患者可行淋巴结清扫术后放疗,继而再选择性进行化疗等。除局部治疗外,化疗是很重要的全身治疗手段。NCCN指南推荐化疗可应用于有症状的具有播散性特征的患者,PS评分0-2分,或无症状的侵袭性强的CUP患者。化疗方案的选择应根据肿瘤的病理学分型(腺癌、鳞癌、神经内分泌肿瘤)。例如铂类为基础的方案常用于转移性鳞癌的治疗,尤其是5-氟尿嘧啶联合顺铂方案是最常用的联合化疗方案;具体治疗方案还要参考转移部位。
CUP的基因组学研究进展
近年来,随着基因组学的研究进展,对CUP目前的趋势是使用二代测序方法确定肿瘤的分子特征,并制定个性化的治疗方案,而不是根据组织类型。2015年发表在《JAMA Oncology》的研究,采用Foundation Medicine开发的全面基因组测序(Comprehensive Genomic Profiling,CGP)对200例CUP组织标本进行检测[1]。其中,腺癌125例、非腺癌75例。在192个(96%)组织标本中,至少检测到1个基因变异,每个肿瘤的平均变异基因数为4.2。文章详细描述了腺癌及非腺癌特异性的变异图谱,见下图。最常见的基因变异为TP53 (110 [55%]),KRAS (40 [20%]),CDKN2A (37[19%]),MYC (23 [12%]),ARID1A (21 [11%]),MCL1 (19[10%]),PIK3CA (17 [9%]),ERBB2 (16[8%]),PTEN (14 [7%]),EGFR (12 [6%]), SMAD4 (13 [7%]),STK11 (13 [7%]),SMARCA4 (12[6%]),RB1 (12 [6%]),RICTOR (12 [6%]),MLL2 (12 [6%]),BRAF (11 [6%]),和BRCA2 (11 [6%])。
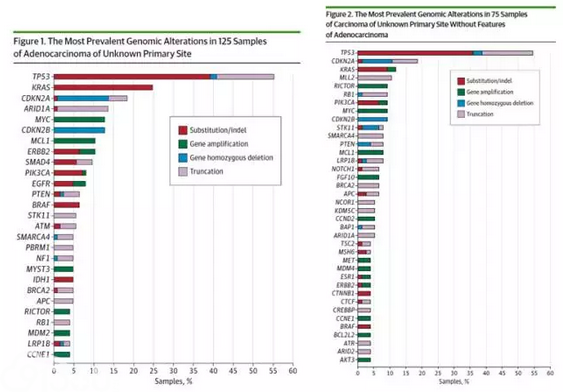
200例肿瘤标本中,169例(85%)检测到一个或多个潜在可靶向治疗的基因变异。在13例(10%)腺癌患者中,检测到ERBB2的突变或扩增率,发生率高于非腺癌患者(3例[4%])。此外,腺癌患者中EGFR(10例[8%] vs 2例[3%]))和BRAF(8例[6%] vs 3例[4%])的变异也更常见。值得注意的是,受体酪氨酸激酶(RTK)/RAS/MAPK信号通路的变异包括ALK、ARAF、BRAF、EGFR 、FGFR1、FGFR2、KIT、KRAS、MAP2K1、MET、NF1、NF2、NRAS、RAF1、RET和ROS1,腺癌(90例[72%])的发生率显著高于非腺癌(29例[39%])。这一研究结果显示,几乎所有的CUP患者,都拥有至少一个临床有意义的基因变异,从而进行个体化治疗。此外,腺癌患者中,RTK/Ras/MAPK通路活化的发生率显著高于非腺癌。文中报道了一例患者检测到MET扩增,接受克唑替尼有较好的应答。全面基因组测序为CUP提供了新的治疗思路,有望改变CUP既往治疗手段有效,预后差的治疗现状。
CUP的肿瘤突变负荷检测
免疫治疗是当下的研究热点,来自多个瘤种的研究证实,肿瘤突变负荷(TMB)可以预测免疫治疗的疗效。既往关于CUP肿瘤突变负荷检测的研究较少,TMB的检测有望为CUP的免疫治疗探寻思路。在今年的ASCO大会上,一项研究报道采用CGP检测CUP的TMB[2]。这一研究从含有10,2878例的常规临床检测组织标本库中筛选出6116例CUP标本进行测序。TMB定义为一份肿瘤样本中,所评估的基因编码区每兆碱基中发生的碱基的置换和插入/缺失突变的总数。根据TMB的高低分为3组:高TMB组(≥20 mut/Mb),中TMB组(≥6 且<20 mut/Mb);低TMB组(6< mut/Mb)。对肿瘤标本数大于100例的肿瘤类型进行分析见下表。
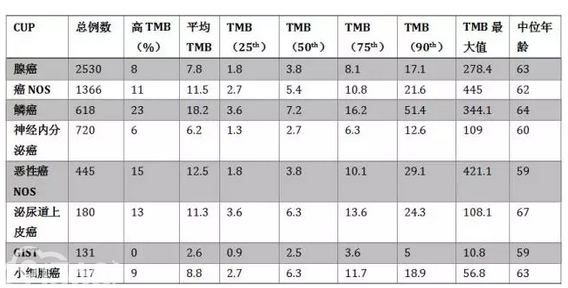
表1 不同类型CUP的TMB
注:25th,50th,75th,和90th分别指百分位数。
该研究显示,除GIST外的不同类型CUP,均有一定比例患者有较高的TMB,提示这些患者有可能从免疫治疗中获益。与预期一致,泌尿道上皮癌患者的平均TMB较高,且高TMB组的患者比例也较高。鳞癌和组织学未定型患者中,高TMB的比例分别为23%和15%。腺癌或癌-未定型是最常见的CUP类型,高TMB患者的比例为8%-11%。总体看来,有10.1%的CUP存在高TMB(≥20 mut/Mb),30.1%的CUP存在中等程度TMB(≥6 且<20 mut/Mb),1.6%的CUP存在MSI-High,提示免疫治疗机会。研究正在进一步分析这类患者对免疫治疗的疗效。
总结
由于大多数的CUP的不良预后和对治疗的抵抗,CUP的诊断和治疗一直以来都是亟待解决的难题。过去对CUP的研究更多集中在明确患者的组织学类型,从而选择可能敏感的治疗方案。近年来,对癌症基因学特征的研究和靶向治疗的应用提示我们,CUP的治疗可以基于其分子特征而非单纯组织学类型。本次ASCO的研究报道,发现有很大比例的CUP患者有较高的TMB,预示其可能从免疫治疗中获益。
专家点评
由于原发灶不明转移癌的异质性,既往通过传统的前瞻性随机对照研究来探寻新疗法,以及利用免疫组化检测来寻找组织起源等重要问题的研究进展缓慢。测序技术的进步,加速了我们对癌症基因特征的认识。创新性试验设计,如篮子试验提示我们,来源于不同组织部位,而拥有相同基因变异的肿瘤,有可能从同样的靶向治疗中获益,这为CUP的治疗提供了新思路。采用全面基因组测序,探寻CUP的基因变异和潜在的治疗靶点是目前研究的热点,不过需要注意的是同样的变异在不同瘤种中的治疗作用差异很大,如BRAF突变的恶性黑色素瘤患者和同样具有BRAF突变的肠癌患者对vemurafenib的治疗效果差异极大。其中的机理值得进一步探索。近年来,免疫治疗的进展如火如荼,在多个瘤种中取得了显著进展。遗憾的是,关于免疫治疗的最佳疗效预测因子,目前尚无定论。多个瘤种的研究提示,肿瘤突变负荷可以预测免疫治疗的疗效。ASCO报道的这一研究,对6000多例不同组织学类型的CUP进行TMB检测,结果显示有相当部分CUP患者有较高的TMB,提示这部分患者非常有可能从免疫治疗中获益。这一研究结果相当鼓舞人心,期待免疫治疗能给CUP的治疗带来重要变革。
参考文献:
1.NCCN Guidelines Version 2.2017, Occult Primary
2.Ross JS, Wang K, Gay L, et al. Comprehensive Genomic Profiling of Carcinoma of Unknown Primary Site: New Routes to Targeted Therapies. JAMA Oncol. 2015,1(1):40-9.
3.J Clin Oncol 35, 2017 (suppl; abstr 3039)




 苏公网安备 32011402010112号
苏公网安备 32011402010112号