
前言:为响应健康中国2030要求,推动全国肿瘤病理诊断能力提升、质量控制,由北京健康促进会发起并主办的“星光生辉—肿瘤规范化病理示范活动”专题推文活动将于近期在91360智慧病理网旗下多个自媒体平台发行举办。活动以肺癌、结直肠癌、乳腺癌、胃癌四大恶性肿瘤为重点开展,以基层肿瘤诊疗规范化建设、肿瘤诊断标准规范流程等内容进行专家专访或解读为主,通过详细的学术分享以促进医院肿瘤诊疗规范化及病理医生肿瘤诊断能力提升。
肺癌的正确诊断和鉴别诊断以及病理类型的分类对肺癌患者的治疗具有重要价值。肺癌的准确分型依赖于病理阅片。病理医生在阅片过程中需要掌握的一些策略可有助于正确诊断,减少不必要的错误。人工智能的发展极大地推动了医学相关学科的进步。本文主要介绍在肺癌病理诊断过程中需要掌握的一些策略,同时也介绍了人工智能在病理诊断中的应用。
肺癌是当今世界严重危害人类健康的常见恶性肿瘤,但随着对肺癌尤其是肺腺癌驱动基因的研究,靶向这些驱动基因改变的药物大大延长了肺癌患者的生存期。肺癌的正确诊断及病理分型有赖于病理医生的正确阅片。作为一名病理医生,应该如何阅片才能正确诊断肺癌?人工智能的发展未来是否可应用于肺癌的病理诊断?
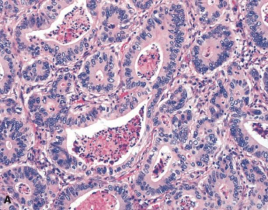
图1 肺转移性结直肠癌
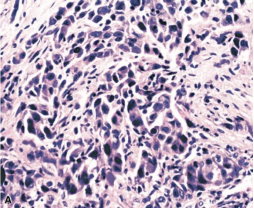
图2 肺转移性乳腺癌
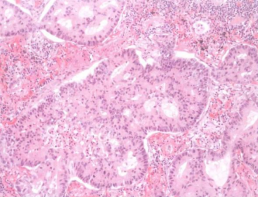
图3 肺浸润性腺癌
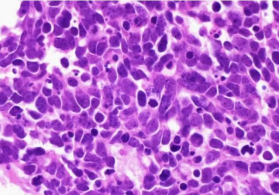
图4 肺小细胞癌
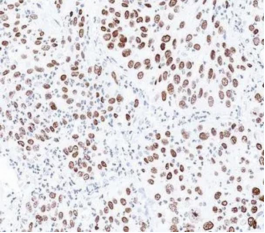
图5 肺鳞癌表达p40
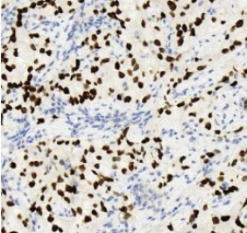
图6 肺腺癌表达TTF1
1 肺癌病理阅片策略
1.1 了解病史很重要 无论是肺穿刺活检标本还是手术切除标本,了解病史非常重要,因为肺是人体其他部位恶性肿瘤最常见的转移部位。身体其他部位恶性肿瘤转移到肺可拟似肺原发性肿瘤。如结直肠癌转移至肺形态学与肺肠型腺癌相同,肺转移性乳腺癌可类似于肺实体型腺癌(图1,2),肺转移性恶性黑色素瘤可沿肺泡壁生长类似于贴壁性腺癌等。

图1 肺转移性结直肠癌

图2 肺转移性乳腺癌
1.2 准确进行肺癌组织学分型 肺癌的组织学分型采用2021年版WHO肺肿瘤组织学分型标准,主要分为鳞状细胞癌、腺癌、大细胞癌和神经内分泌癌等【1】(图3,4)。WHO肺肿瘤分类对每种类型肿瘤的组织学形态均进行了详细的描述,病理医生应根据每种肿瘤的组织学形态进行病理诊断。

图3 肺浸润性腺癌

图4 肺小细胞癌
1.3 合理选择免疫标记 对于分化差的肺恶性肿瘤,仅仅依靠形态学难以明确分类,此时需要选用适当的免疫标记帮助诊断。目前支持肺鳞癌的标记物有p40、p63和CK5/6(图5),肺腺癌的标记物有TTF1和NapsinA(图6),CgA、Syn和INSM1等支持神经内分泌癌的诊断。大细胞癌是一种排除性诊断,需要在细胞形态、组织结构、免疫组化等方面缺乏神经内分泌癌、鳞癌、腺癌,以及巨细胞癌、梭形细胞癌和多形性癌的特点。

图5 肺鳞癌表达p40

图6 肺腺癌表达TTF1
肺是全身肿瘤的常见转移部位,应注意除外转移性肿瘤。免疫组化有助于鉴别组织来源,如肺(TTF1和NapsinA)、乳腺(GCDFP15、Mammaglobin和GATA3)、肾细胞癌(PAX8和RCC)、胃肠道(CDX2和villin)、前列腺(NKX3.1和PSA)以及间皮(WT1。Calretinin、D2-40)等【2】。
1.4 精准报告各种病理参数 对于手术切除标本,不仅给出明确的肿瘤病理类型外,还应准确报告肿瘤是否存在气腔内扩散、有无淋巴结转移和胸膜侵犯,为临床提供准确的TNM分期,从而指导临床治疗。
2 肺癌病理阅片的未来展望
随着新的技术发展,未来的肺癌病理诊断并不仅囿于传统的显微镜下观察。近些年来人工智能在医学领域中的作用越来越大,在肺癌的诊断、治疗和预后等方面也发挥着重要的作用
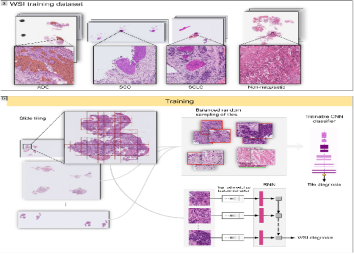
2.1 肺癌的精准诊断 一项研究发现采用深度学习模型对小的经支气管肺活检标本中的肺癌进行分类,训练的模型能对83例不确定病例进行独立的分类,AUC达到了0.99。在肺癌的细胞学诊断中,有研究发现采用深度卷曲神经网络(DCNN)技术可使70%图像正确分类,该研究结果提示DCNN在细胞学诊断中的肺癌分类有价值【3,4】。

2.2 肺癌肿瘤微环境分析 肿瘤微环境现在越来越多的研究被认为在恶性肿瘤的进展和治疗中发挥重要作用,肿瘤组织内不同细胞类型的空间构造显示肿瘤微环境具有重要信息。一项研究采用基于组织学的数字染色切片和基于深度学习的计算机模型对肺腺癌HE染色切片上的肿瘤细胞核、间质、淋巴细胞、巨噬细胞、核碎裂和红细胞进行分析。使用该工具他们确定和分类细胞核,并提取48个细胞空间结构相关特征。研究者使用这些特征开发了一个预后模型,并对TCGA肺腺癌数据集进行独立验证,结果发现高风险组比低风险组预后明显差,而且图像来源的肿瘤微环境特征明显与生物通路的基因表达相关,如T细胞受体和PD1通路等【5】。
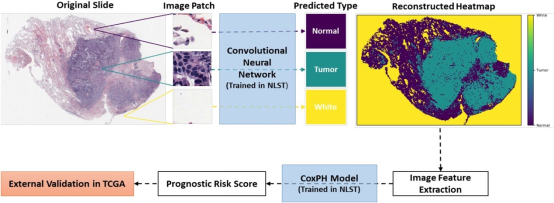
2.3 肺癌预后评估 一项研究发现,采用深度卷曲神经网络技术开发的一种用于肺癌病理图像的自动化肿瘤区域识别系统,他们提取22个定义明确的形态和边界特征,发现其中15个明显与肺腺癌病人的生存结局相关。预测的高风险组的预后明显差于低风险组。预测的风险分组在调整年龄、性别、吸烟和分期后是一个独立的预后因素【6】。

总之,肺癌的病理诊断不仅涉及到HE染色切片的形态学观察,同时还需要借助免疫组化标志物进行正确的病理分型。人工智能的技术发展,在肺癌的病理诊断等方面发挥了较大的作用,将来人工智能技术可能会成为病理医生的一个重要的辅助手段在包括肺癌等疾病中发挥不可磨灭的作用。
参考文献·
1. WHO Classification of Tumours Editorial Board. Thoracic Tumours. 5th ed. Lyon (France): International Agency for Research on Cancer 2021.
2. 中华医学会肺癌临床诊疗指南(2022版)。中华医学杂志,2022,102(23):1706-1740.
3. Kanavati F, Toyokawa G, Momosaki S, et al. A deep learning model for the classification of indeterminate lung carcinoma in biopsy whole slide images. Sci Rep,2021,11(1):8110.
4. Teramoto A, Tsukamoto T, Kiriyama Y, et al. Automated classification of lung cancer types from cytological images using deep convolutional neural networks.Biomed Res Int, 2017,2017:4067832.
5. Wang S, Rong R, Yang DM, et al. Computational staining of pathology images to study the tumor microenvironment in lung cancer. Cancer Res, 2020,80(10): 2056-2066.
6. Wang S, Chen A, Yang L, et al. Comprehensive analysis of lung cancer pathology images to discover tumor shape and boundary features that predict survival outcome. Sci Rep, 2018,8:10393.
7. Coudray N, Ocampo PS, Sakellaropoulos T, et al. Classification and mutation prediction from non-small cell lung cancer histopathology images using deep learning. Nat Med, 2018,24(10): 1559-1567.




 苏公网安备 32011402010112号
苏公网安备 32011402010112号