近年来,肿瘤免疫治疗取得了令人瞩目的成果,可改善部分肿瘤患者的预后,显著延长患者的生存期。2018年被称为中国免疫治疗的元年,与此同时,肿瘤免疫治疗生物标志物的探索也成为了治疗研究的热点,如何筛选获益人群、预测治疗有效性迫在眉睫,其中PD-L1、TMB、dMMR / MSI检测研究较多,本期91360特邀北京协和医院吴焕文教授就dMMR/MSI-H在预测免疫治疗中的价值进行采访。

1 dMMR /MSI-H是当前临床肿瘤治疗中的一个热点话题,尤其是近几年研究发现可以作为免疫治疗的预测生物标记物,您可以简单介绍一下dMMR /MSI-H吗?
吴焕文教授:DNA错配修复( mismatch repair,MMR)是DNA损伤修复机制的主要类型之一,可以纠正DNA复制、基因重组过程中产生或外源性损伤造成的碱基错配、插入及缺失。MMR基因胚系/体细胞突变和MLH1基因甲基化可以导致DNA MMR功能缺陷,使得相应的MMR蛋白表达缺失,进而引起DNA复制错误的累积。DNA MMR功能正常为pMMR(proficient mismatch repair),DNA MMR功能缺陷即dMMR(deficient mismatch repair)。
免疫组化(Immunohistochemistry,IHC)检测MMR蛋白表达情况可以用来反应DNA MMR功能状态。MMR蛋白表达完整/正常为pMMR;MMR蛋白表达缺失/异常为dMMR。
微卫星( microsatellite,MS) 是指以少数几个核苷酸( 多为1~6个) 为单位串联重复的DNA序列,又称短串联重复( short tandem repeat,STR) ,在基因组中广泛分布。上述DNA MMR功能缺陷引起的DNA复制错误在基因组的微卫星位点中尤为明显,致使微卫星长度发生改变(少数核苷酸的插入或缺失),该现象被称为微卫星不稳定性(microsatellite instability,MSI)。根据程度将MSI分为3类:微卫星高度不稳定性( MSI-high,MSI-H)、微卫星低度不稳定性( MSI-low,MSI-L) 、微卫星稳定( microsatellite stability,MSS)。MSI-H对应于dMMR,而MSI-L、MSS则对应于pMMR。
dMMR/MSI-H在不同瘤种的发生率存在较大差异,在结直肠癌、子宫内膜癌、胃癌、小肠癌中发生率较高,在卵巢癌、肝胆管癌、上泌尿道癌、肾上腺皮质癌等肿瘤中也有一定的发生率。
2 dMMR/MSI-H可以作为免疫治疗的预测生物标志物,主要根据哪些临床研究?
吴焕文教授:近年来临床研究提示,相当一部分的dMMR/MSI-H 表型晚期实体瘤对于免疫检查点抑制剂(如PD-1/ PD-L1抗体)治疗具有显著疗效。如:CheckMate-142研究(一项多中心、多队列、开放、非对照II期临床研究, 入组的患者为组织学确诊的复发性结直肠癌或转移性结直肠癌患者)发现纳武利尤单抗( nivolumab)联合伊匹木单抗( ipilimumab)在dMMR/MSI-H患者中显示出显著的临床疗效,且患者的疗效与PD-L1表达,BRAF/KRAS突变状态无关。这一研究结果提示,纳武利尤单抗联合伊匹木单抗可以作为dMMR/MSI-H转移性结直肠癌患者新的治疗选择。基于这些研究,经美国食品药品监督管理局( Food and Drug Administration,FDA) 批准,纳武利尤单抗分别于2017年和2018年获批单药及联合低剂量伊匹木单抗治疗其他后线治疗无效的dMMR/MSI-H晚期/转移性结直肠癌患者。另有KEYNOTE-016研究提示,dMMR/MSI-H可以有效预测晚期实体瘤患者是否从免疫检查点抑制剂治疗中受益,且与具体癌种无关。基于此,FDA于2017年批准帕博利珠单抗( pembrolizumab) 用于先前治疗后进展、无满意替代治疗方案的dMMR/MSI-H晚期/转移性实体瘤患者,dMMR/MSI-H也因此成为跨癌种的明星标志物。
虽然目前国内获批的肿瘤免疫检查点抑制剂药物暂无dMMR/MSI-H肿瘤适应症,但随着国内相关临床研究的不断开展以及相关适应症的不断拓展,dMMR/MSI-H在免疫治疗疗效预测中的作用会受到越来越多的重视。
3 dMMR/MSI-H作为预测免疫治疗的生物标志物,如何检测?
吴焕文教授:MMR IHC检测与DNA MSI检测是不同的实验手段,检测MMR功能缺陷导致的不同生物学效应。在结直肠癌、子宫内膜癌中两者的检测结果高度一致。
免疫组化(Immunohistochemistry, IHC)检测4个MMR蛋白(MLH1、PMS2、MSH2、MSH6)表达情况。肿瘤细胞核4个MMR蛋白表达完整/正常为pMMR;肿瘤细胞核一个或者多个MMR蛋白表达缺失/异常为dMMR。
DNA MSI检测可以用PCR或NGS方法。MSI 的PCR检测方法一般按National Cancer Institute(NCI)工作组推荐的5个位点(单核苷酸重复序列:BAT25, BAT26;双核苷酸重复序列:D2S123,D5S346,D17S250)进行检测。也可考虑全部采用单核苷酸重复序列(BAT-25,BAT-26, NR-21, NR-24, MONO-27或/和NR-27)。5个位点中, 2个或2个以上有不稳定性归为MSI-H,1个位点不稳定归为MSI-L,没有位点不稳定则归为MSS。
不论哪种方法在临床应用前都需要经过严格的性能验证并通过相关机构审批。
4 dMMR/MSI-H在检测过程中还要注意哪些问题?
吴焕文教授:确实,在dMMR/MSI-H检测中还有很多需要注意的地方。
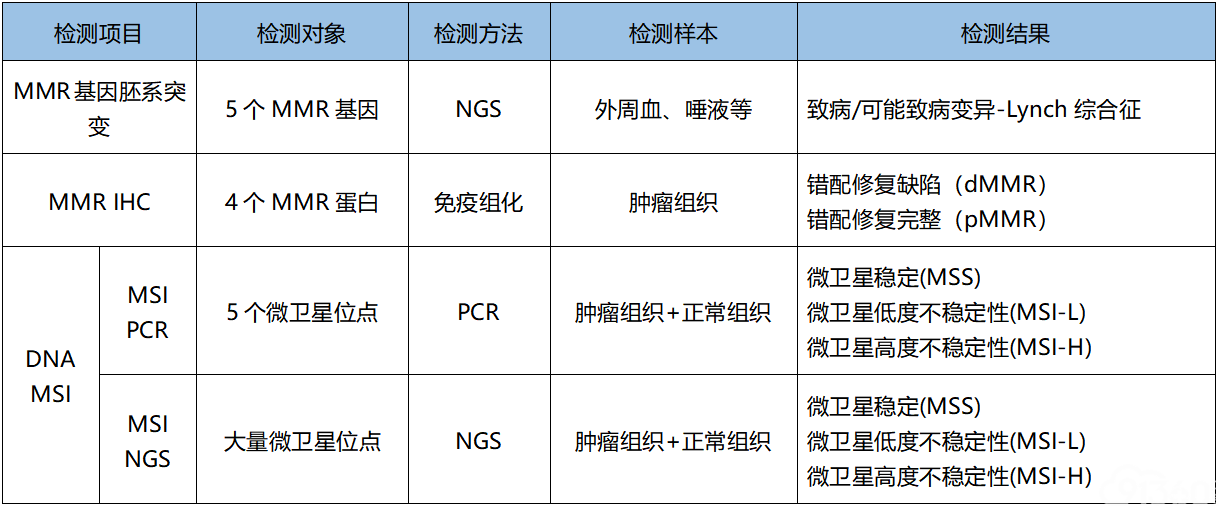
首先,要明确相关概念(可参考附表)。dMMR/MSI-H不等同于Lynch综合征,MLH-1基因启动子区域高甲基化或MMR基因体细胞突变等原因也可导致dMMR/MSI-H。dMMR/MSI-H是Lynch综合征筛查手段,Lynch综合征的确诊依赖于MMR基因(EPCAM, MLH1, PMS2, MSH2, MSH6)胚系突变检测。MMR IHC检测与DNA MSI检测是不同的实验手段,检测MMR功能缺陷导致的不同生物学效应。在实际应用中,为了避免概念混淆,最好不要把MMR IHC检测看成MSI的检测方法之一。
其次,理论上MMR IHC与DNA MSI(PCR或NGS)检测结果应具有高度一致性。但是每种方法都具有明显的优点与局限,实际工作中有时候需要互相补充。MMR IHC检测受到新辅助治疗、标本前处理及染色过程的影响。最为重要的是,病理医师需要了解并掌握MMR蛋白的特定判读标准,避免参照既往常规免疫组化判读方式或标准进行MMR IHC结果判读。DNA MSI检测对肿瘤细胞占比要求较高,检测方必须具备相关的病理质控措施。另外,DNA MSI检测不能反映肿瘤异质性状态。DNA MSI检测时还需要留意微迁移(minimal microsatellite shift)的准确解读(尤其是子宫内膜癌)。
另外,在MSI发生率较低的肿瘤中,MMR IHC与DNA MSI(PCR或NGS)检测结果间的一致性尚需进一步探索。
5 如何更加精准地应用dMMR/MSI-H预测免疫治疗?
吴焕文教授:首先,应该意识到dMMR/MSI-H的重要意义,加强与临床医师的沟通与交流,积极开展相关检测,满足临床与患者需求。其次,推动人员培训,实现检测与结果判读规范化,做好实验室质控。在此基础上,积极开展科研探索,推动更加精细化的治疗策略制定。
NP/IO/4693/05/26/20-05/26/22




 苏公网安备 32011402010112号
苏公网安备 32011402010112号