慢性髓性白血病(CML,常称为慢性粒细胞白血病)是骨髓造血干细胞克隆性增殖形成的恶性肿瘤,常以外周血白细胞异常升高及中性中、晚幼粒及成熟粒细胞、嗜酸性粒细胞、嗜碱性粒细胞增多为其特征。95%以上的患者具有Ph染色体,所有的CML都有BCR和ABL1基因重排。
以伊马替尼为代表的酪氨酸激酶抑制剂(TKI)作为一线治疗药物使CML患者的10年生存率达85%~90%,尼洛替尼、达沙替尼等二代TKI一线治疗CML能够获得更快更深的分子学反应,亦成为CML患者的一线治疗药物选择。TKI治疗获得持续稳定的深度分子学反应超过2年以上的患者,部分能够获得长期的无治疗缓解(TFR,treatment free remission,),即功能性治愈。异基因造血干细胞移植(allo-HSCT)曾经是CML的一线治疗方案,但供者来源、患者年龄、移植相关风险等多种因素限制其应用,逐步成为TKI治疗失败或不耐受后的二线甚至三线治疗选择。在CML的治疗中应该在详细评估患者的全面情况后,向其推荐优先治疗药物选择,参考患者的治疗意愿,进行下一步治疗。
二、诊断技术和应用
(一)高危人群的监测筛查
CML约占成人白血病的15%,全球年发病率约为(1.6~2)/10万人。我国年发病率为(0.36~0.55)/10万人。随着年龄增加,CML发病率有逐步升高的趋势。美国低于20岁人群年发病率大约0.2/10万,80~90岁人群年发生率增加至10/10万,中位发病年龄67岁;欧洲患者中位年龄为60岁。中国CML患者较西方更为年轻化,国内几个地区的流行病学调查显示CML中位发病年龄45~50岁。CML致病的病因比较复杂,较为公认的因素是电离辐射,暴露于辐射的人群有较高的CML发病率。没有证据表明其他因素与CML的相关性。
(二)临床表现
1.症状
CML起病缓慢,其自然病程包括慢性期、加速期及急变期。70%患者是在症状出现之后方去就诊并得以诊断。部分患者在体检或其他原因检验血细胞计数时才发现血液异常。90-95%的患者初诊时为慢性期。
慢性期患者主要临床表现为贫血和脾脏肿大相关的症状。包括疲乏无力、消瘦、萎靡不适、纳差、早饱感、左上腹或腹部的疼痛不适等。早期一般无出血症状,后期约有30%患者表现不同程度的出血,如鼻出血、齿龈出血、皮肤瘀斑、消化道出血、视网膜出血等。女性可有月经过多。颅内出血少见。出血原因与血小板减低(少见)或血小板功能异常有关。少数患者出现血小板及白细胞显著增高导致栓塞及其相关症状,例如脾梗塞引起的左上腹急性剧烈疼痛,阴茎异常勃起。部分患者存在尿酸增高导致的痛风性关节炎,嗜碱性粒细胞增多导致组胺释放过多引起消化道溃疡。尽管CML慢性期患者白细胞显著升高,部分大于100×109/L,但患者出现心肺血管白细胞淤滞相关症状并不常见。白细胞淤滞相关症状包括:肺动脉淤滞导致的气短、脑血管淤滞引起的嗜睡、运动协调能力减低或丧失、头晕症状等。
CML疾病进展包括加速期和急变期,其临床表现是一个循序渐进、逐渐加剧的过程,难以绝对分开,并且约有20%~25%的患者不经加速期而直接进入急变期。进展期患者消耗性症状增加,例如不明原因的发热、乏力、纳差、盗汗、消瘦加重等,部分出现头痛、骨关节疼痛,伴有与白细胞不成比例的脾脏迅速肿大伴压痛,淋巴结突然肿大,贫血常进行性加重;急变期患者除伴有上述症状外还可出现髓外浸润表现,如皮肤结节,睾丸浸润,阴茎异常勃起,眼眶浸润出现绿色瘤等。急变患者出现严重感染、出血症状,危及生命。急变以急髓变多见,大约占60%,急淋变大约占30%,10%的患者急变为急性巨核细胞白血病或未分化急性白血病。少数CML患者急变表现为髓外原始细胞浸润,骨髓及外周血仍然显示出典型的慢性期状态。最常见的部位是淋巴结、皮肤和软组织、乳腺、胃肠道、泌尿道等,骨骼及中枢神经系统也可受累。
2.体征
脾脏肿大和面色苍白是最常见的临床体征,40%~70%患者在初诊时脾脏肿大,脾脏肿大程度不一,轻则肋下刚及,重则达脐部,甚至于盆腔。脾肿大程度与患者病情、病程及白细胞数密切相关。腹部触诊通常无触痛,如有脾周围炎可有触痛或摩擦感。胸骨压痛也是常见的体征,通常局限于胸骨体,因触痛而拒绝按压。肝脏肿大患者少见,比例不超过10%。慢性期患者淋巴结肿大、皮肤及其他组织浸润少见,淋巴结肿大以颈部、锁骨上窝及腋窝多见,但通常不大,只有少数患者直径在1cm以上。进展期患者出现淋巴结等组织器官浸润的相关体征。
(三)辅助检查
1.外周血细胞分析
白细胞数升高是本病的显著特征,诊断时白细胞通常在25×109/L以上,一半以上患者白细胞高达100×109/L以上,未治疗的患者白细胞进行性升高。白细胞数增加与脾脏肿大呈正相关性。分类中可见到各阶段原始及幼稚粒细胞,形态基本正常;嗜酸性粒细胞、嗜碱性粒细胞比例/绝对值增加。中性粒细胞功能轻度异常,粒细胞数量的显著升高可弥补粒细胞功能的缺陷,因此慢性期患者罕有发生常见或机会型感染。
血红蛋白及红细胞早期可正常,血片中可以见到少量有核红细胞,尤其是合并骨髓纤维化的患者。网织红细胞正常或偏高,临床溶血罕见。疾病发展过程中因出血、溶血、骨髓红细胞生成减少而出现血红蛋白下降。贫血多为正细胞正色素性。红细胞改变很少,部分出现红细胞分布宽度增加,红细胞畸形罕见,例如椭圆形或不规则性红细胞。
血小板多数增高或正常,50%患者血小板在诊断时升高,部分可达1000×109/L以上,增高程度与白细胞水平无相关性。血小板形态正常,功能多异常,尽管血小板升高,但血小板升高相关的血栓性事件少见,血小板功能异常相关的出血事件亦少见;少数患者血小板可减少。
CML患者诊断时淋巴细胞总数升高,主要是T辅助和T抑制细胞数增加,脾脏的T淋巴细胞亦增加。B淋巴细胞数无明显增加。
2.骨髓细胞形态学
骨髓明显增生或极度增生,造血细胞占骨髓细胞的75%~90%,以粒系增生为主,红细胞及淋巴细胞相对减少,粒∶红常为10~30∶1,甚至50∶1(正常情况下粒细胞:红细胞为2-4:1)。慢性期患者分类以近成熟阶段粒细胞为主,嗜酸性粒细胞、嗜碱性粒细胞比例升高,可见幼稚阶段的嗜碱及嗜酸性粒细胞。粒细胞形态可异常,表现为核浆发育不平衡,颗粒多少不一。红系统、淋巴细胞、单核系统比例相对减低。巨核细胞数可增高也可正常,在一张涂片上可见数百或上千个巨核细胞,易见小巨核细胞。巨核细胞形成血小板良好,涂片中血小板不少,可成堆分布。进展期患者骨髓出现原始细胞比例显著增多。
骨髓活检:非必须检测项目。部分患者活检显示骨髓纤维化,尤其是病程长并且未进行有效治疗的患者以及进展期患者。
3.中性粒细胞碱性磷酸酶
外周血或骨髓的中性粒细胞碱性磷酸酶(ALP)水平明显减低,约90%左右CML患者粒细胞缺乏此酶。ALP减低与Ph染色体阳性无相关性,但可因病情进展到急变期或感染而出现升高,也可随治疗好转而增加。在明确BCR-ABL、JAK2突变对CML、PV等MPN诊断意义后,ALP活性不再作为CML与PV等疾病的鉴别手段。
4.细胞遗传学
遗传学证据是确定CML诊断的必备条件。细胞遗传学检查发现Ph染色体或BCR、ABL1基因重排(bcr/abl1融合基因)存在均可确定CML的诊断。常规细胞遗传学检查是最常用的检测手段,95%的患者常规染色体分析可发现Ph染色体而明确诊断,部分患者可检测到Ph染色体以外的核型异常。荧光原位杂交(FISH)是一项敏感、精确的检测BCR、ABL1基因重排技术,在部分核型正常的患者采用FISH方法证实BCR/ABL1重排明确诊断。
变异型Ph染色体:见于5%的患者,往往形成复杂易位(累积3条或以上染色体),除Y染色体以外其他染色体均可累及。在变异型Ph染色体中,22q?存在,但缺失的部分易位至9号染色体以外染色体,或形成累及9、22、其他染色体的复杂遗传物质互换。高分辨率技术(High-resolution techniques)分析显示无论经典还是复杂的Ph染色体, 9q34与22q11融合是Ph染色体形成的根本。
隐匿性Ph染色体: 9q34与22q11互换易位,9q34易位至22q11形成光学显微镜下22q-、9q+,光学显微镜下22q-是Ph染色体的辨认标志,少数情况下,易位后22q-相比经典型在光镜下加长而无法辨认,即所谓隐匿性Ph染色体,此时通过显带技术和分子学方法明确BCR-ABL的重排。
慢性期大约70%患者为经典Ph染色体,20%患者合并有其他染色体异常,包括?Y、+8、 22q?、+Ph等。-Y在60岁以上正常人群比例为10%。
5.分子学
来自9号染色体ABL1基因3’端片段易位至22号染色体并与BCR基因5’端片段融合形成bcr/abl1融合基因,转录为8.5kb的RNA转录本,翻译成为210kDa并具有酪氨酸激酶活性的融合蛋白p210 BCR/ABL。因断裂位点不同,bcr/abl融合基因片段长度及翻译形成蛋白大小有所差异。在CML,BCR常见有3个断裂点区域:M-bcr, m-bcr, u-bcr。其中主要断裂点簇区M-bcr,可产生2种形式的bcr/abl融合转录本:e13a2(b2a2), e14a2(b3a2),蛋白产物皆为P210(p210 BCR-ABL);发生于次要断裂点m-bcr与abl第二外显子形成e1a2融合转录本,翻译成P190蛋白(p190 BCR-ABL)。此种形式发生在超过50%的Ph+急性淋巴细胞白血病(ALL)中;若bcr断裂位点位于M-bcr下游,命名为μ-bcr,形成e19a2转录本,蛋白产物为P230(p230BCR-ABL)。绝大多数CML患者融合蛋白为p210 BCR-ABL,可同时表达p190 BCR-ABL,少数患者单纯表达p190 BCR-ABL或p230 BCR-ABL。
RT-PCR(反转录-聚合酶链反应)是检测bcr/abl融合基因的重要方式,定量RT-PCR技术可以检测出10-6~10-4水平的残留白血病细胞,不仅是确定诊断,也是治疗反应评价的重要手段。
7.生化检查
常见乳酸脱氢酶升高,尿酸升高亦常见,合并肝肾损害是可出现相关指标异常。
(四)CML的诊断标准
典型的临床表现、体征和(或)血液骨髓细胞检查异常,必需有Ph染色体和(或)有bcr/abl融合基因阳性方可确定诊断。
(五)鉴别诊断
CML诊断基础在于遗传学检查发现Ph染色体和(或)bcr/abl融合基因,这也成为CML与下述疾病鉴别的关键。
1.早期的慢性粒细胞白血病应与粒细胞类白血病反应相鉴别
粒细胞类白血病反应是机体应激而发生的类似于白血病的血象变化。常见的原因为感染、中毒、癌肿、大出血、急性溶血、休克和外伤等。尤以感染和癌肿较多见。类白血病反应主要鉴别点为:①去除病因,类白血病反应会消失;②无胸骨压痛,脾不大或轻度肿大;③通常无贫血及血小板减少;④白细胞增多型类白血病反应白细胞可超过50×109/L。一般在100×109/L以内,超过200×109/L罕见;⑤类白血病反应者中幼粒细胞百分率不高,原粒少见,嗜酸性粒细胞低于正常;⑥嗜酸性粒细胞类白血病中血及骨髓中以成熟嗜酸性粒细胞为主;⑦粒细胞胞质中有明显的中毒颗粒和空泡,缺乏白血病细胞异型性、核浆发育不平衡等特征。⑧中性粒细胞碱性磷酸酶(N-ALP)活性增高。⑨无Ph染色体或BCR-ABL融合基因。
2.CML与其他骨髓增殖性肿瘤鉴别
慢性粒细胞白血病与真性红细胞增多症、原发性骨髓纤维化及原发性血小板增多症同属于骨髓增殖性肿瘤范畴。在其发病过程及临床表现方面有着相似的临床特征,且可以相互转化。
真性红细胞增多症以红细胞增多为突出表现,伴有红细胞增多所致高粘血症,并多有脾肿大等临床表现;白细胞轻度增多,但一般不超过50×109/L;血小板也有轻度增加,红细胞容量明显超过正常值。N-ALP高,Ph染色体或bcr/abl融合基因为阴性,95%患者检测到JAK2V617F突变。
原发性血小板增多症以血小板增多为主(>450×109/L)同时伴有血小板功能异常。白细胞轻度增多,多在50×109/L以下;嗜酸性粒细胞、嗜碱性粒细胞不增多。脾脏轻度肿大,中性粒细胞碱性磷酸酶增高,无Ph染色体或bcr/abl融合基因,约50%患者检测到JAK2V617F突变。
原发性骨髓纤维化时患者多有贫血,脾多肿大且肿大程度与白细胞数不成比例,即脾肿大显著而白细胞仅轻度增多,或因脾功能亢进白细胞反而减少。外周血中易见幼稚粒细胞及有核红细胞,原始细胞及各阶段幼粒细胞甚至比骨髓中的比例还要多。成熟红细胞形态显著异常,有泪滴样改变或月牙形及盔甲形等。骨髓活检有确诊价值。无Ph染色体或bcr/abl融合基因,约50%患者检测到JAK2V617F突变。
3.CML与其他慢性白血病鉴别
CML还应与慢性中性粒细胞白血病(CNL)、慢性嗜酸性粒细胞白血病、嗜碱性粒细胞白血病、慢性粒单核细胞白血病(CMML)、不典型CML相鉴别。
CNL少见,病情进展缓慢,白细胞增高以成熟中性粒细胞为主,N-ALP增高,无Ph染色体或BCR-ABL融合基因,且极少发生急性变。
嗜酸、嗜碱性粒细胞白血病分别以各阶段嗜酸性或嗜碱性粒细胞增多为主要表现,且伴有嗜酸、嗜碱细胞形态异常。CML急变期或加速期可发生嗜碱性粒细胞比例增多,若CML发生嗜酸性粒细胞或嗜碱性粒细胞急性变时,嗜酸或嗜碱性粒细胞比例应超过30%,且各阶段中幼粒、嗜酸粒或嗜碱性粒细胞比例增多,并伴有原始粒细胞和早幼粒细胞增多。
CMML、不典型CML目前归类于骨髓增殖性肿瘤/骨髓增生异常综合征的范畴,但其临床特点及骨髓象极似CML,CMML除具有单核细胞增多的特点外,CMML及不典型CML无Ph染色体或BCR-ABL融合基因。
4.其他
CML的脾肿大还应与肝硬化、血吸虫病、黑热病、霍奇金病、肝糖原累积病等引起的脾大相鉴别。CML合并脾梗死引起的左上腹剧痛应与相关急腹症相鉴别。但由于本病有特殊血象,鉴别并不困难。
(六)CML分期
1.慢性期
① 外周血(PB)或骨髓 (BM)中原始细胞<10%。
② 没有达到诊断加速期或急变期的标准。
2.加速期
①外周血(PB)或骨髓 (BM)中原始细胞占10%~19%。
②血中嗜碱细胞≥20%。
③与治疗不相关的持续血小板减少(<100 x 109/L)或增高(>1000 x 109/L)。
④克隆演变。
⑤进行性脾脏增大或WBC计数增高。
3.急变期
①外周血(PB)或骨髓(BM)中原始细胞≥20%。
②骨髓活检原始细胞集聚 。
③髓外原始细胞浸润。
(七)CML预后分层
许多因素影响CML的慢性期及生存期。目前常用的评分系统包括Sokal、Euro以及EUTOS(表1),均以临床特点以及血液学指标作为预后评分因素。目前无明确数据判断三种预后积分系统的优劣,无论采取何种预后评估方式,建议对高危的患者采用更为积极的治疗和监测。
表1 CML-CP预后评分系统
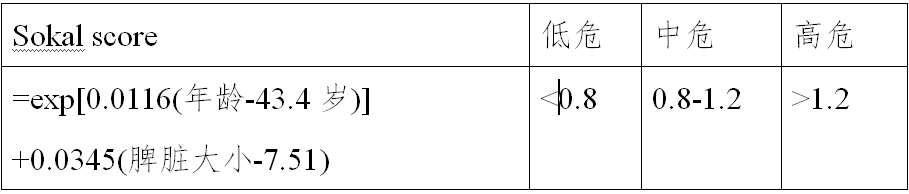
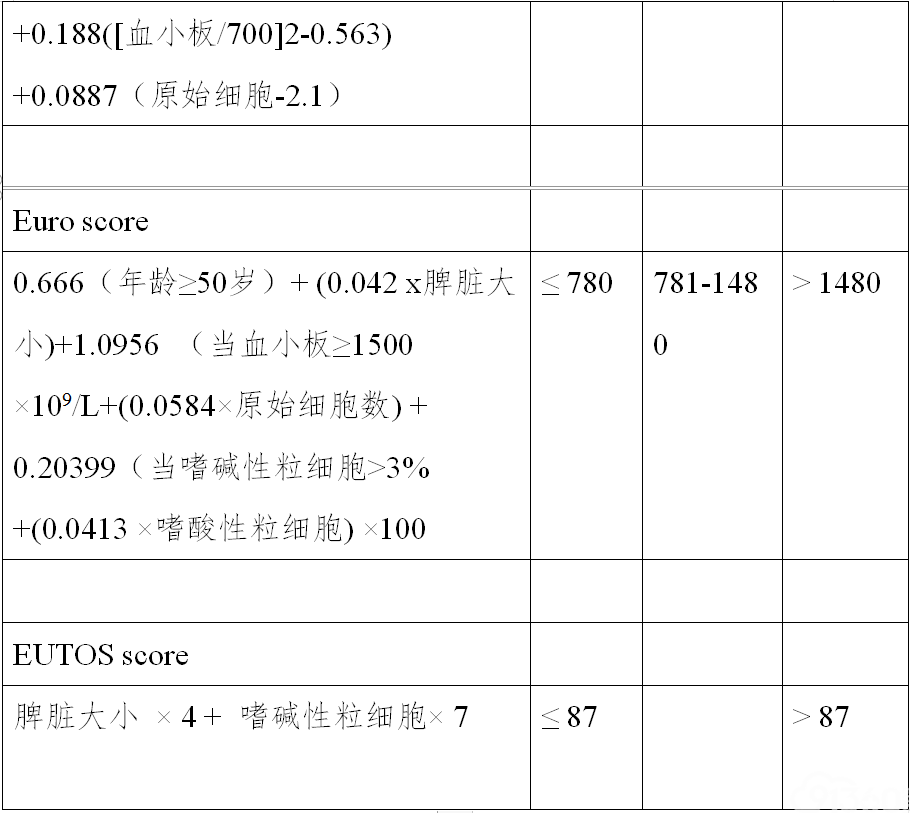


血小板计数(×109/L),年龄为岁数,脾大小为肋下厘米数,原始细胞、嗜酸性粒细胞、嗜碱性粒细胞为外周血分类百分数。所有数据应当在任何CML相关治疗开始前获得。
四、治疗
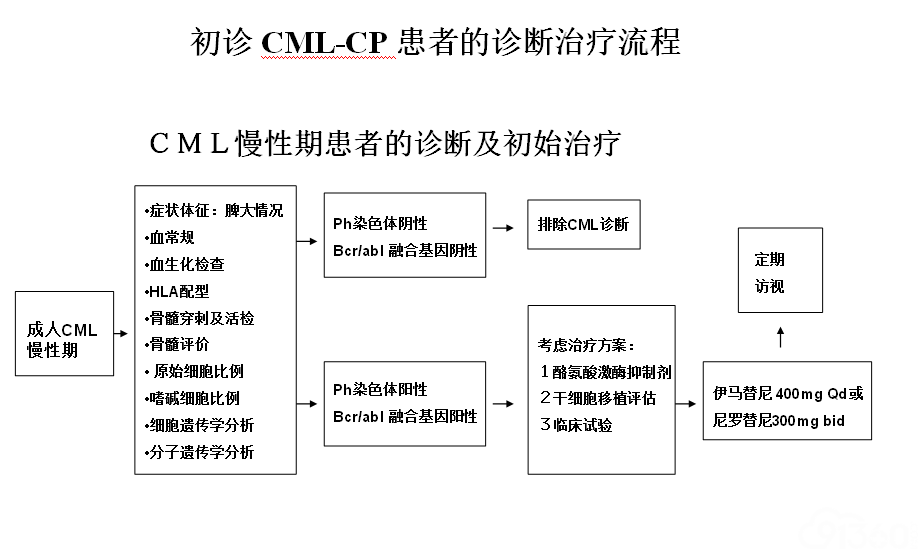
(一)新诊断CML-CP患者的初始治疗:
CML治疗经历了放疗、化疗、免疫治疗、骨髓移植、分子靶向治疗等一系列治疗措施,疗效逐渐提高。放疗、化疗以改善症状为主,无法改变CML自然病程。二十世纪七十年代异基因造血干细胞移植使得CML可以治愈,但受年龄和供者的限制仅约三分之一患者有条件接受移植,并且移植物抗宿主病、感染、复发一直是制约移植疗效的三大难题。二十世纪八十年代初干扰素的应用约可使10~20%患者获得细胞遗传学完全缓解,以干扰素为基础的治疗成为九十年代缺乏移植条件的CML患者的治疗首选。二十世纪九十年代末酪氨酸激酶抑制剂(TKI)甲磺酸伊马替尼(Imatinib mesylate, IM)成功用于临床,成为CML治疗的里程碑,CML的治疗进入了分子靶向治疗时代。2008年国际上已公认伊马替尼是CML慢性期的一线治疗,干扰素不再推荐作为CML的主要治疗选择,异基因移植退出CML一线治疗。随着二代、三代TKI的出现,CML一线治疗TKI选择更多样,异基因造血干细胞移植也成为CML二、三线治疗的选择。依据患者的自身状况及预后分层采用个体化的恰当治疗方案是提高疗效、延长患者生存期最根本有效方法。
1.酪氨酸激酶抑制剂治疗
(1)一线TKI药物种类
目前国际指南推荐新诊断CML慢性期患者的一线治疗药物包括伊马替尼400mg/天,尼洛替尼600mg/天(300mg,2次/天),达沙替尼100mg/天。获得中国SFDA批准的一线治疗药物为伊马替尼和尼洛替尼。三种药物一线治疗的近期和远期疗效见表2。
表2 三种一线TKI药物疗效比较
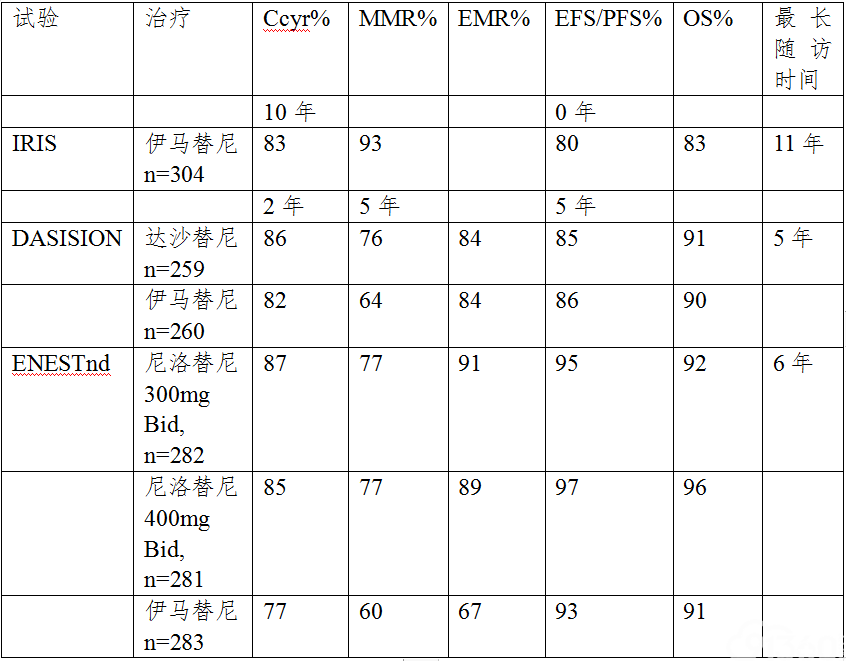

(2)如何选择一线治疗药物
新诊断CML-CP治疗选择多样,在规范监测和正确支持治疗情况下TKI耐受性良好。伊马替尼、尼洛替尼的不良反应存在差异,因此患者的基础状况在药物选择上是重要的影响因素。
伊马替尼治疗部分不良反应严重影响生活质量,包括体重增加、疲乏无力、外周及眶周水肿、骨骼肌肉疼痛、恶心等。多数为低级别轻度到中度,5-10%长期治疗患者出现肌酐升高。
尼洛替尼治疗导致部分患者血糖升高、脂肪酶升高,对于未得到有效控制的糖尿病或胰腺炎病史患者,应当谨慎处方尼洛替尼。临床前研究显示尼洛替尼可能延长心电图的Q-T间期,因此尼洛替尼治疗开始前检测心电图(Q-T间期),保证血钾、血镁在正常范围;尼洛替尼治疗期间仍应监测心电图、血钾、血镁。尼洛替尼应当空腹服用,避免进食尤其是高脂肪饮食后导致的尼洛替尼血药浓度增加。尼洛替尼增加血管痉挛或血管阻塞性事件发生率,包括已报道的心肌梗塞、脑梗塞、外周动脉闭塞性疾病等。ENESTnd研究随访6年数据显示,大约10%患者发生血管事件。因此对于存在糖尿病、冠状动脉疾病、脑动脉血管疾病高风险因素的患者应谨慎使用尼洛替尼作为一线治疗,存在上述疾病史的患者避免使用尼洛替尼。尼洛替尼每日2次空腹使用可能降低药物治疗依从性。
尽管尼洛替尼在内的二代TKI早期治疗反应显著优于伊马替尼,但目前研究并未显示二代TKI一线治疗的长期生存获益,可能与伊马替尼一线治疗失败后二代、三代TKI甚至移植作为有效的挽救治疗方案相关。目前认为二代TKI的主要优势在于降低高危患者的疾病进展。因此,对于高危患者可选择二代TKI作为初始治疗选择。二代TKI能够使更多患者获得稳定的深度分子学反应(DMR)进而成功停止TKI治疗获得TFR。小于50岁的年轻患者因生存期长,考虑到终生服药带来的经济负担、低级别副反应对生活质量的影响,TFR成为这部分患者治疗的目标。相比伊马替尼,二代TKI的一线治疗诱导DMR具有显著优势。因此对年轻患者可优先考虑二代TKI一线治疗。对于老年患者,高质量的长期生存相比DMR和TFR显得更为重要。
(3)治疗反应监测
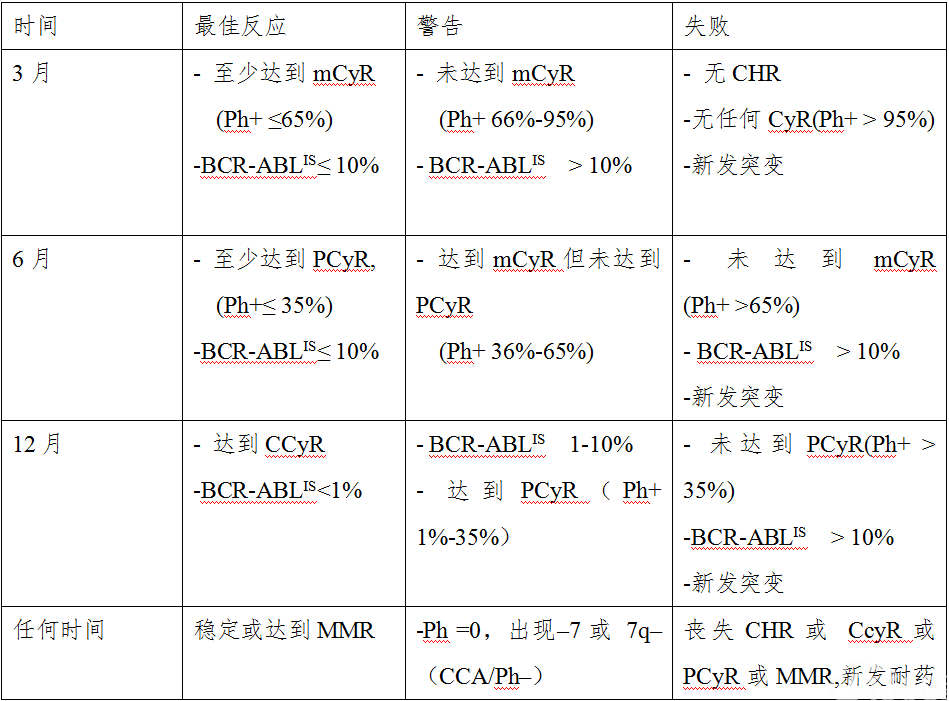
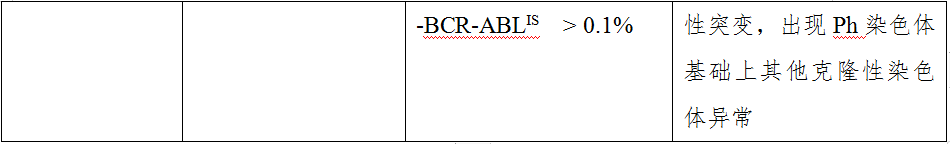
治疗期间应定期监测血液学、细胞及分子遗传学反应,定期评估患者TKI治疗耐受性,参照中国CML诊疗指南(2016)推荐反应标准(表3)进行治疗反应评估(表4)。早期的分子学反应(EMR)至关重要,特别是TKI治疗三个月的BCR-ABL水平。临床治疗反应包括最佳反应、治疗失败以及警告。血液学、细胞遗传学以及分子学监测参照表5进行。分子学反应评估采用外周血检测BCR-ABL1转录本水平,建议使用BCR-ABLIS来反映BCR-ABL(P210)转录本水平以正确评价患者疗效。建议实验室在检测体系稳定后尽早获得有效的转换系数(CF)以转换BCR-ABLIS,并通过定评估即室间质控样品比对校正来保证CF持续准确。此外,CF仅适用于具有P210型BCR-ABL、转换后BCR-ABLIS<10%CML患者的转换。
表3 治疗反应的定义
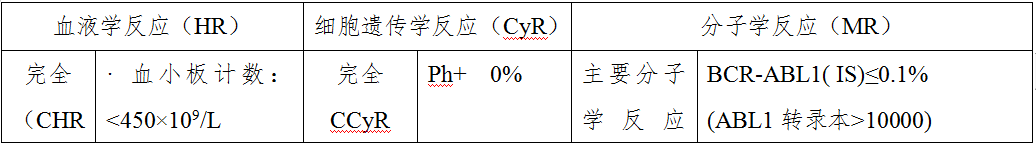
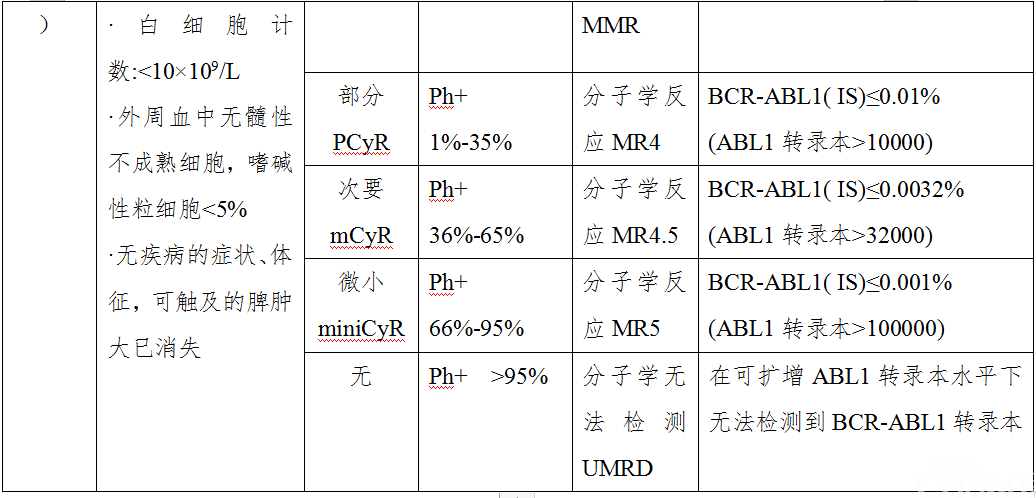
表4 一线TKI治疗CML-CP患者治疗反应评价标准
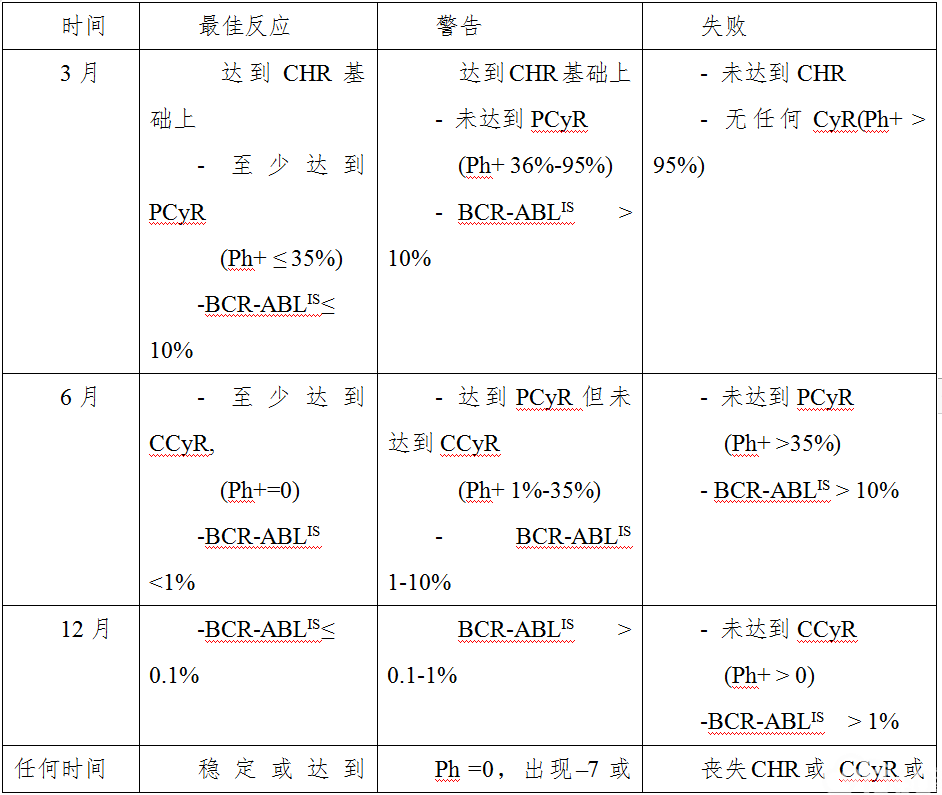
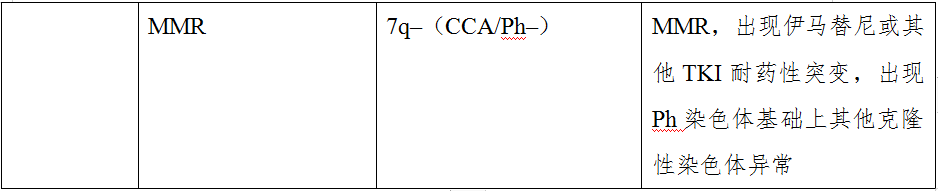


表4 一线TKI治疗CML-CP患者治疗反应评价标准


(附注:CHR:完全血液学缓解;CyR:细胞遗传学反应;PCyR:部分细胞遗传学反应;CCyR:完全细胞遗传学反应;MMR主要分子学反应; IS:国际标准化。)
表5 TKI治疗反应监测推荐
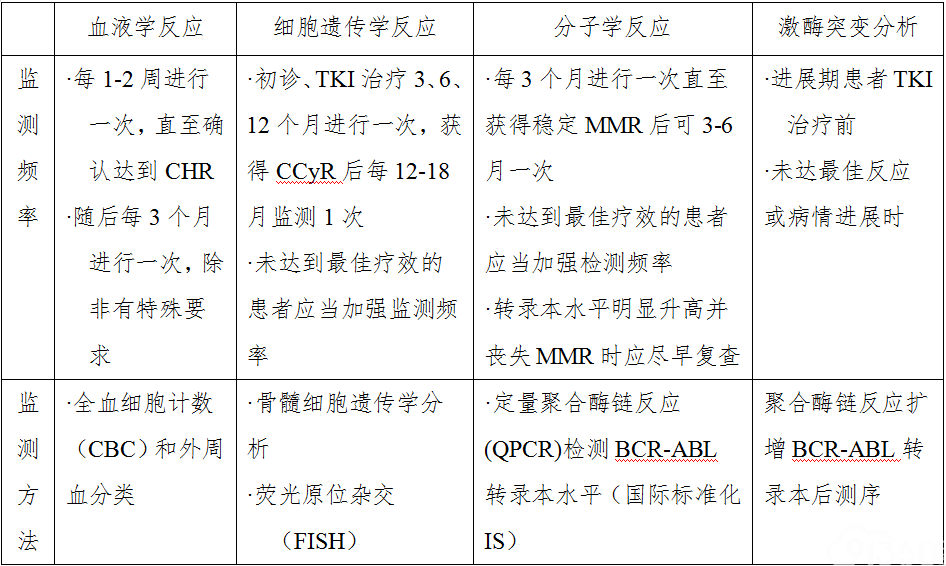

(二)CML-CP患者一线TKI治疗不满意患者策略调整
治疗失败以及警告的患者在评价治疗依从性、患者的药物耐受性、合并用药的基础上及时行bcr/abl激酶区突变检测,适时更换其他TKI(表6)。二线TKI选择可参照如下原则:
1.应综合考虑患者病史、合并症、合并用药、药物不良反应以及药物说明书并结合BCR-ABL激酶突变类型选择。
2.参照BCR-ABL激酶突变类型:目前以下7种类型突变对于达沙替尼或尼洛替尼选择具有较为明确的指导意义。
(1)T315I:二者均耐药,有条件者可进入临床试验,或选择恰当的治疗方案。
(2)F317L/V/I/C,V299L,T315A:采用尼洛替尼治疗更易获得临床疗效。
(3)Y253H,E255K/V,F359C/V/I:采用达沙替尼治疗更易获得临床疗效
二线TKI治疗患者反应评估参照表7进行。二代TKI治疗失败的患者可考虑行异基因干细胞移植。频繁、长期的TKI治疗中断以及患者服药依从性差的问题可能导致不良临床结果,一线TKI耐受不佳的患者应及时更换TKI。良好服药依从性教育以及严密监测对于获得最佳临床疗效非常重要。
表6 一线TKI治疗CML-CP患者治疗调整策略
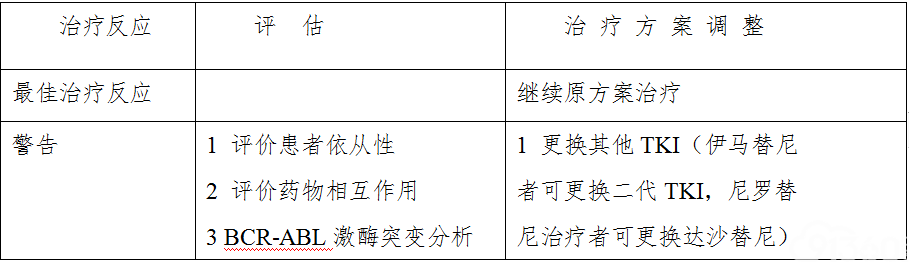
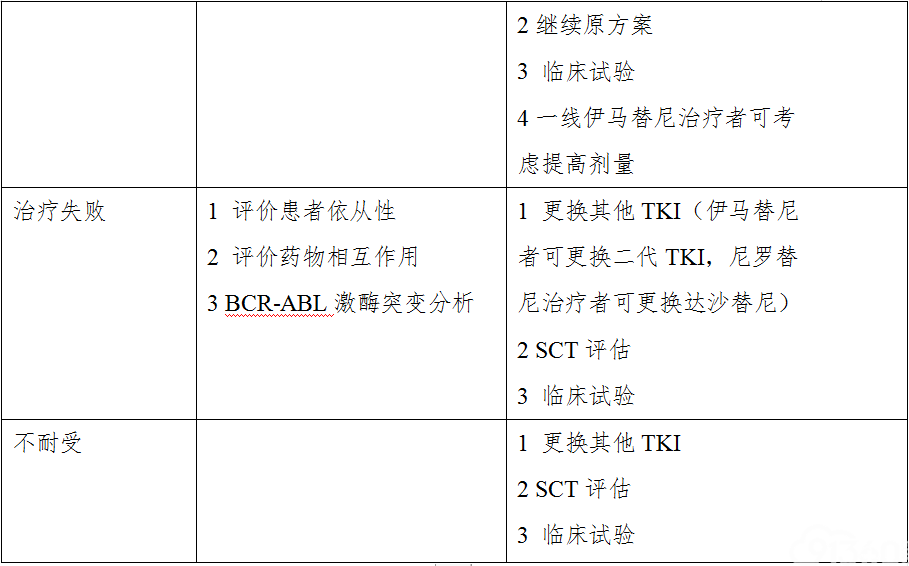


表7 二线TKI治疗CML-CP患者治疗反应评价标准


(附注:CHR:完全血液学缓解;CyR:细胞遗传学反应;mCyR: 次要细胞遗传学反应;PCyR:部分细胞遗传学反应;CCyR:完全细胞遗传学反应;MMR主要分子学反应; IS:国际标准化。)
(三)新诊断CML-CP的其他治疗:
因各种原因无法使用TKI治疗的患者可考虑以下治疗方案。
1.干扰素为基础的方案
在CML的TKI治疗时代,干扰素为基础的治疗方案逐步成为二三线选择。结合中国的实际情况,以下患者可考虑干扰素为基础的方案:TKI耐药、不耐受且不适合SCT的CML慢性期患者;各种原因暂时无法应用TKI治疗的或无法坚持长期使用TKI的慢性期患者。
2.异基因造血干细胞移植(Allo-SCT)
异基因干细胞移植依然是CML治疗的重要手段,尤其是TKI耐药以及进展期患者。在TKI治疗时代移植不再是CML慢性期患者的一线治疗选择,原则上对至少一种二代TKI不耐受或耐药的患者考虑异基因干细胞移植。因此Allo-SCT作为二线TKI治疗失败后的三线的治疗选择,目标人群包括①标准的伊马替尼治疗失败的慢性期患者,可根据患者的年龄和意愿考虑行Allo-SCT。②治疗任何时候出现ABL基因T315I突变的患者,首选Allo-SCT。③二代TKI治疗反应欠佳、失败或不耐受的所有患者。④更换二代TKI6个月后仍未获得主要遗传学反应者,其12个月获得MCyR以及长生存的可能性明显降低,应尽早考虑Allo-SCT。⑤加速期或急变期的患者。
(四)CML进展期患者治疗
1.加速期治疗:参照患者既往治疗史、基础疾病以及BCR-ABL激酶突变情况选择适合的TKI,病情回复至慢性期者,可继续TKI治疗,如果患者有合适的造血干细胞供者来源,可考虑行Allo-HSCT。存在T315I突变或二代TKI不敏感突变的患者应及早行Allo-SCT。有条件进行新药临床试验的单位可行新药试验。
2.急变期治疗:参照患者既往治疗史、基础疾病以及突变情况选择TKI单药或联合化疗提高诱导缓解率,缓解后应尽快行Allo-SCT。有条件进行新药临床试验的单位可行新药试验。
五、停止TKI治疗
伊马替尼为代表的TKI治疗显著改善了CML的预后,是药物靶向治疗人类恶性肿瘤的成功典范。随着患者生存期的显著延长,越来越多的研究者开始关注长期TKI治疗毒副反应对患者生活质量的影响,每日坚持用药对多数患者而言成为艰难挑战,长期治疗对国家和个人造成的经济负担。停用TKI成为解决上述问题的最佳方式。近年来一系列的临床研究证实部分获得持续深度分子学反应的患者能够实现相对持久的安全停药(TFR)。
1.TFR可能性:
最早的停药研究是法国的pilot试验。12例长期接受伊马替尼治疗获得至少2年的完全分子学反应(CMR)的患者尝试停药,中位随访7.5年(4.4-8.4年),50%的患者维持持续的分子学反应。法国STIM试验入组100例伊马替尼治疗获得CMR持续2年以上患者,停止伊马替尼治疗12月TFR达到41%,累积60个月TFR高达39%。STIM2临床试验显示停止伊马替尼治疗24个月TFR为46%。澳大利亚白血病与淋巴瘤协作组进行TWISTER试验24个月TFR为47.1%。目前全球范围进行前瞻或回顾性停药试验数据显示,伊马替尼或二代TKI治疗或DMR2年以上患者停止TKI治疗后TFR在40-60%。
2.TFR停药标准:
目前的停药实验数据显示获得持续MR4/MR4.5以上分子学反应,并且持续超过2年是目前停药试验的前提条件,仅仅获得完全细胞遗传学反应或主要分子学反应的患者停药后均出现迅速的分子学复发。
3.复发并启动再次治疗标准
随着停药试验数据的增多逐步发生变化。早期的停药试验以CMR为停药标准,复发标准为丧失CMR或MMR。ASTIM试验以MMR的丧失作为复发再治疗标准,31%患者停药随访期间出现转录本水平波动,但均在低于0.1%。所有丧失MMR患者接受伊马替尼或二代TKI治疗再次获得分子学反应,仅1例患者再次获得MMR后出现疾病进展。ASTIM试验提示以MMR丧失作为再治疗的标准的临床可行性。其他伊马替尼停药、二代TKI停药数据显示以丧失MMR作为复发再治疗标准在临床可行并且安全。
4.复发后再治疗效果
无论是研究者还是患者均关注TKI治疗停止后复发的再治疗药物选择和疗效。无论是前瞻性的法国STIM系列试验、TWISTER试验、二代TKI停药试验,还是美国、日本的回顾性数据分析,结果均显示TKI治疗获得持续深度分子学反应后停药后复发的患者,对停药前的TKI再治疗敏感,能够再次获得良好的分子学反应,包括主要和深度分子学反应。
5.临床及生物学指标预测成功停药
除了分子学反应深度和持续时间之外,还有其他因素影响停药能否成功。STIM和TWISTER研究中回顾性分析影响成功停药的因素,研究发现,相对于Sokal高危患者,低危患者以及停药前持续伊马替尼治疗时间长的患者更易实现成功停药。Yhim及研究者在小样本的研究中证实低危患者在停止伊马替尼治疗后更易维持持续的分子学反应。日本回顾性停药研究和ASTIM试验结果显示既往接受干扰素治疗的患者具有更高的停药成功率。部分研究提示NK细胞介导的免疫耐受与TKI停药后疾病控制相关。
6.停药患者筛选:
美国癌症综合网(NCCN)2017CML指南对于停止TKI治疗提出明确建议。建议临床试验外,满足下列条件尝试停药:大于18岁、慢性期患者并且TKI治疗超过三年以上;可进行国际标准化定量的BCR/ABL(P210)转录本;稳定深度分子学反应超过2年;既往无TKI耐药;有条件接受严格规范的国际标准化的分子学监测,分子学结果解读正确迅速;在有经验的临床医师的指导进行TFR尝试;能够获得及时再治疗以及正确的再治疗后分子学监测。
附件1:
附件1:
责任编辑: WZ






 苏公网安备 32011402010112号
苏公网安备 32011402010112号